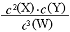题目内容
某温度时,在一个2 L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间变化的曲线如图所示。下列有关该反应的叙述中不正确的是
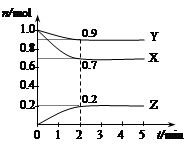
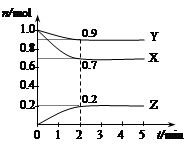
A.化学方程式为X(g)+3Y(g) 2Z(g) 2Z(g) |
B.从反应开始至2 min,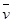 (X)=0.075 mol ·L-1· min-1 (X)=0.075 mol ·L-1· min-1 |
| C.2min后该反应在此条件下已达到化学平衡 |
| D.若X、Y、Z均为气体,反应达平衡时的压强是开始时的0.9倍 |
A
试题分析:根据图像可知,反应进行到2min时,各种物质的物质的量浓度不再发生变化,说明反应达到平衡状态,C正确;平衡时X和Y的物质的量分别减少了0.3mol、0.1mol,Z的物质的量增加了0.2mol,则反应的化学方程式是3X(g)+Y(g)
 2Z(g),A不正确;从反应开始至2 min,用X表示的反应速率是
2Z(g),A不正确;从反应开始至2 min,用X表示的反应速率是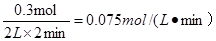 ,B正确;若X、Y、Z均为气体,反应达平衡时的压强是开始时的
,B正确;若X、Y、Z均为气体,反应达平衡时的压强是开始时的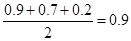 倍,D正确,答案选D。
倍,D正确,答案选D。点评:该题是基础性试题的考查,试题难易适中,侧重对学生基础知识的巩固与训练,主要是考查学生对可逆反应限度的熟悉程度,以及灵活运用基础知识解决实际问题的能力。该题的关键是记住可逆反应的限度和反应速率的含义和表达式,然后结合图像灵活运用即可。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 2NO2(g);△H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示。下列说法正确的是( )
2NO2(g);△H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示。下列说法正确的是( )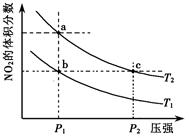
 HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅
HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅
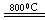 2MgCl4+Ti在Ar气氛中进行的理由是____________________。
2MgCl4+Ti在Ar气氛中进行的理由是____________________。 CH3OCH3(g)+H2O(g) ΔH=" -23.5" kJ/mol
CH3OCH3(g)+H2O(g) ΔH=" -23.5" kJ/mol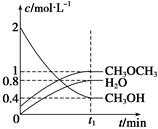
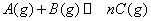
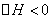 ,在不同条件下反应混合物中C的质量分数C%和反应过程所需时间的关系曲线,有关叙述一定正确的是
,在不同条件下反应混合物中C的质量分数C%和反应过程所需时间的关系曲线,有关叙述一定正确的是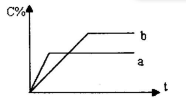
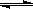 2/3Fe (s)+CO2(g),已知该反应在不同温度下的平衡常数如下。则:
2/3Fe (s)+CO2(g),已知该反应在不同温度下的平衡常数如下。则:
 2SO3(g),△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;若增大压强时,反应速度变化情况画在c-d处。
2SO3(g),△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;若增大压强时,反应速度变化情况画在c-d处。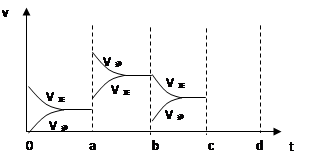
 2NH3已达到平衡状态( )
2NH3已达到平衡状态( )