题目内容
已知某反应的能量变化如图所示,下列说法正确的是
| A.该反应可用于表示烧碱与硫酸反应 |
| B.该反应只有在加热条件下才能进行 |
| C.反应物的总能量高于生成物的总能量 |
| D.该反应可用于表示碳酸钙受热分解的反应 |
D
解析试题分析:由图可知:反应物的能量低,生成物的能量高,由反应物发生反应变为生成物时要从环境中吸收热量。该反应为吸热反应。A.烧碱与硫酸反应是放热反应。错误。B.该反应只有在一定条件下发生,但是反应不移动要在加热条件下。错误。C.反应物的总能量低于生成物的总能量。错误。D.碳酸钙受热分解的反应是吸热反应,因此改图可表示这一反应。正确。
考点:考查反应的热效应的判断及应用的知识。

练习册系列答案
相关题目
白磷会对人体造成严重的烧伤,白磷(P4)分子结构为 。下列说法不正确的是
。下列说法不正确的是
| A.白磷着火点低,在空气中可自燃 |
| B.白磷、红磷互为同素异形体 |
| C.31 g白磷中,含P—P键1.5 mol |
| D.已知P4(白磷,s)+3O2(g)===2P2O3(s) ΔH=-Q kJ·mol-1,则白磷的燃烧热为Q kJ·mol-1 |
已知 H2(g) +Cl2(g) =2HCl(g)反应放出热量为Q1,H2(g) +Br2(g)= 2HBr(g)反应放出热量为Q2有关上述反应的叙述正确的是( )
| A.Q1<Q2 |
| B.生成物总能量均高于反应物总能量 |
| C.生成1 mol HCl气体时放出Q1热量 |
| D.1 mol HBr(g)具有的能量大于1 mol HBr(l)具有的能量 |
2013年6月11日我国成功发射了“神州十号”。这标志着中国人的太空时代又前进了一大步。发射“神十”时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。已知:
N2(g)+2O2(g)=2NO2(g);△H=+67.7 kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534 kJ/mol
下列关于肼和NO2反应的热化学方程式中,正确的是
| A.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l);△H=-1135.7 kJ/mol |
| B.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=-1000.3 kJ/mol |
| C.N2H4(g)+NO2(g)=3/2N2(g)+2H2O(l);△H=-1135.7 kJ/mol |
| D.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=-1135.7 kJ/mol |
对于化学反应中的能量变化,表述准确的是
| A.形成新化学键的过程会放出能量 | B.中和反应是吸热反应 |
| C.加热才能发生的反应是吸热反应 | D.生成CO2的反应是放热反应 |
沼气是一种能源,它的主要成分是CH4。0.5molCH4完全燃烧生成CO2和液态水时放出445kJ的热量,则下列热化学方程式中正确的是
| A.2CH4(g) + 4O2(g) =2CO2(g) + 4H2O(l) ΔH=+890kJ·mol-1 |
| B.CH4(g) + 2O2(g) =CO2(g) + 2H2O(l) ΔH=+890kJ·mol-1 |
| C.CH4(g) + 2O2(g) =CO2(g) + 2H2O(l) ΔH=-890kJ·mol-1 |
| D.1/2CH4(g) + O2(g) =1/2CO2(g) + H2O(l) ΔH=-890kJ·mol-1 |
下列说法不正确的是
A.NH3·H2O NH4++OH-达到平衡后,升高温度平衡正向移动 NH4++OH-达到平衡后,升高温度平衡正向移动 |
| B.在海轮的外壳上镶入锌块,可减缓船体的腐蚀速率 |
| C.明矾水解生成Al(OH)3胶体,可用作净水剂 |
| D.如图所示的反应过程中A+B→X的△H<0,X→C的△H>0 |
关于下列各图的叙述中不正确的是
| A.已知CO的燃烧热为283 kJ/mol,2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ/mol,则图甲表示CO和H2O(g)生成CO2和H2的能量变化 |
| B.某温度下,pH=11的NH3·H2O和pH=1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+ 、NH3·H2O与NH3三种微粒的平衡浓度之和为0.05 mol·L-1 |
| C.在常温下,X2(g)和H2反应生成HX的平衡常数如表所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐渐降低,且X2与H2反应的剧烈程度逐渐减弱 |
D.图乙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中, 的变化情况 的变化情况 |

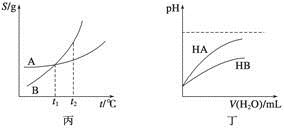
 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态