题目内容
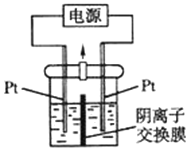
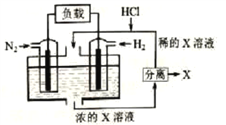
【题目】下图是几种电化学装置,请答下列问题。

(1)图一被保护的钢闸门应与外接电源的_______极相连,这种方法称之为___________;
(2)图二往Fe极区滴入2滴黄色的K3[Fe(CN) 6]溶液,一段时间后的现象________________。
(3)图三烧杯中盛放足量的CuSO4溶液总反应的离子方程式为_____________________;25℃,若起始时盛放100mLpH=5的CuSO4溶液,一段时间后溶液的pH变为1,此时仍只有一个电极上产生气体,若要使溶液恢复到起始时的浓度(忽略溶液体积的变化),可向溶液中加入_____(填写物质的化学式)___________g。
【答案】 负 外加电流的阴极保护法 生成有特征蓝色的沉淀 2Cu2++2H2O![]() 2Cu+O2↑+4H+ CuO (或CuCO3) 0.4 (或0.62)
2Cu+O2↑+4H+ CuO (或CuCO3) 0.4 (或0.62)
【解析】(1)根据图示可知,此电化学防护的方法为外加电源的阴极保护法,即钢闸门、辅助电极和外接电源构成电解池,其中钢闸门做电解池的阴极被保护,辅助电极做阳极,钢闸门做阴极,故应与外接电源的负极相连,该装置的原理是外加电源的阴极保护法,故答案为:负;外加电源的阴极保护法;
(2)滴入2滴黄色K3[Fe(CN)6](铁氰化钾)溶液时,发生反应:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,产生蓝色沉淀;故答案为:产生蓝色沉淀;
(3)乙装置中阳极上氢氧根离子失电子生成氧气,阴极上铜离子得电子生成Cu,其电解反应的离子方程式为:2Cu2++2H2O![]() 2Cu+O2↑+4H+;故答案为:2Cu2++2H2O
2Cu+O2↑+4H+;故答案为:2Cu2++2H2O![]() 2Cu+O2↑+4H+;
2Cu+O2↑+4H+;
③由2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4,要使溶液恢复原状态,可加入CuO(或CuCO3),一段时间后溶液的pH变为1,则c(H+)=0.1mol/L-10-5mol/L=0.1mol/L,n(H+)=0.1L×0.1mol/L =0.01mol,则由电解反应可知析出的Cu的物质的量为0.005mol,由Cu原子守恒可知,m(CuO)=0.005mol×80g/mol=0.4g,或m(CuCO3)=0.005mol×124g/mol=0.62g,故答案为:CuO(或CuCO3);0.4(或0.62)。
2Cu+O2↑+2H2SO4,要使溶液恢复原状态,可加入CuO(或CuCO3),一段时间后溶液的pH变为1,则c(H+)=0.1mol/L-10-5mol/L=0.1mol/L,n(H+)=0.1L×0.1mol/L =0.01mol,则由电解反应可知析出的Cu的物质的量为0.005mol,由Cu原子守恒可知,m(CuO)=0.005mol×80g/mol=0.4g,或m(CuCO3)=0.005mol×124g/mol=0.62g,故答案为:CuO(或CuCO3);0.4(或0.62)。

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案