题目内容
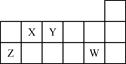
W、X、y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为________________________________________________________________ 。
(2)W与Y可形成化合物W2Y,该化合物的电子式为________。将等体积、等浓度的W
的最高价氧化物对应的水化物和Y的氢化物混合,其化学方程式为__________________。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为_____________________________________________________。
(4)W、X、Y、Z四种元素简单离子的离子半径由小到大的顺序是_______________。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为________________________________________________________________ 。
(2)W与Y可形成化合物W2Y,该化合物的电子式为________。将等体积、等浓度的W
的最高价氧化物对应的水化物和Y的氢化物混合,其化学方程式为__________________。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为_____________________________________________________。
(4)W、X、Y、Z四种元素简单离子的离子半径由小到大的顺序是_______________。
(1)Al(OH)3+OH-=AlO2-+2H2O(2分)
(2)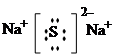 (1分) NaOH+H2S=NaHS+H2O(2分)
(1分) NaOH+H2S=NaHS+H2O(2分)
(3)Cl2+SO2+2H2O=H2SO4+2HCl(2分)
(4)Al3+<Na+< Cl-<S2-(1分)
(2)
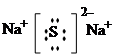 (1分) NaOH+H2S=NaHS+H2O(2分)
(1分) NaOH+H2S=NaHS+H2O(2分)(3)Cl2+SO2+2H2O=H2SO4+2HCl(2分)
(4)Al3+<Na+< Cl-<S2-(1分)
试题分析:(1)W、X是金属元素,且最高价氧化物对应的水化物可以反应生成盐和水,可知W、X分别是Na和Al ,NaOH和Al(OH)3反应生成盐和水。
(2)W与Y可形成化合物W2Y,W是Na,则Y是S, W2Y是Na2S。等物质的量的NaOH和H2S反应生成
NaHS和H2O。
(3) Y的低价氧化物SO2通入Z单质Cl2的水溶液中,发生氧化还原反应,生成H2SO4和HCl。
(4)W、X、Y、Z四种元素分别是Na、Al、S、Cl,所以离子半径由小到大的顺序是Al3+<Na+< Cl-<S2-。

练习册系列答案
 金博士一点全通系列答案
金博士一点全通系列答案
相关题目