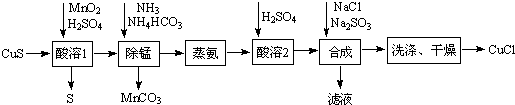
题目内容
6.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )| A. | 28 g乙烯和28g丙烯中均含有6NA对共用电子对 | |
| B. | 标准状况下,2.24L氯仿中含有C-Cl数目为0.3NA | |
| C. | 标准状况下,560 mL甲烷和甲醛的混合气体中,含有的共用电子对数为0.2NA | |
| D. | 11.2L乙烯、乙炔的混合物中C原子数为NA |
分析 A、依据n=$\frac{m}{M}$计算物质的量,结合烯烃结构分析计算电子对数;
B、标况下,氯仿为液态;
C、甲烷和甲醛中分子中都含有4个共价键;
D、气体所处的状态不明确.
解答 解:A、依据n=$\frac{m}{M}$计算乙烯物质的量=$\frac{28g}{28g/mol}$=1mol,1mol乙烯中含有6NA对共用电子对,丙烯物质的量=$\frac{28g}{42g/mol}$,丙烯中含有共用电子对=$\frac{28g}{42g/mol}$×9×NA=6NA,均含有6NA对共用电子对,故A正确;
B、标况下,氯仿为液态,不能根据气体摩尔体积来计算其物质的量,故B错误;
C、标况下560mL甲烷和甲醛的混合气体的物质的量为0.025mol,甲烷和甲醛中分子中都含有4个共价键,0.025mol混合气体中含有0.1mol共价键,含有的共用电子对数为0.1NA,故C错误;
D、气体所处的状态不明确,故气体摩尔体积的数值不明确,无法计算其物质的量和碳原子个数,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
14.0.1mol Na2SO4溶解在( )mol H2O中,才能使100个H2O中含1个Na+.
| A. | 20 mol | B. | 10 mol | C. | 5 mol | D. | 30 mol |
18.2002年诺贝尔化学奖获得者的贡献之一是发明了对有机分子的结构进行分析的质谱法.其方法是让极少量(10-9 g左右)的化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子.如C2H6离子化后可得到C2H6+、C2H5+、C2H4+、…然后测定其质荷比β.设H+的质荷比为1,某有机物样品的质荷比如图(假设离子均带一个单位正电荷,信号强度与该离子多少有关),则该有机物可能( )

| A. | CH3OH | B. | C3H8 | C. | C2H4 | D. | CH4 |
15.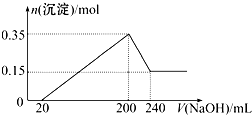 将一定质量的镁和铝混合物投入200mL 硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.则下列说法不正确的是( )
将一定质量的镁和铝混合物投入200mL 硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.则下列说法不正确的是( )
 将一定质量的镁和铝混合物投入200mL 硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.则下列说法不正确的是( )
将一定质量的镁和铝混合物投入200mL 硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.则下列说法不正确的是( )| A. | 镁和铝的总质量为9g | |
| B. | 最初20 mLNaOH溶液用于中和过量的硫酸 | |
| C. | 硫酸的物质的量浓度为2.5mol/L | |
| D. | 镁和铝混合物投入硫酸中生成的氢气在标准状况下的体积为11.2L |