题目内容
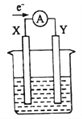
【题目】如图是一氧化碳-空气燃料电池的工作原理示意图,a、b均为惰性电极。下列叙述中,正确的是( )
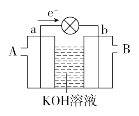
A. a电极发生还原反应,b电极发生氧化反应
B. a电极的电极反应式为CO+4OH-+2e-===CO32-+2H2O
C. A处通入的是空气,B处通入的是CO
D. 用该电池作电源精炼铜,若阴极质量增加6.4 g,至少消耗标准状况下的CO 2.24 L
【答案】D
【解析】
一氧化碳-空气燃料电池,在碱性条件下的总反应是2CO+O2+4OH-=2CO32-+2H2O。
A. 电子由a极流出,a是负极,a电极CO失电子发生氧化反应,b电极氧气得电子发生还原反应,故A错误;
B. a是负极,a电极CO失电子发生氧化反应,a电极的电极反应式为CO+2OH--2e-===CO32-+H2O,故B错误;
C.a是负极,A处通入的是CO,b是正极,B处通入的是空气,故C错误;
D. 用该电池作电源精炼铜,若阴极质量增加6.4 g,则转移电子的物质的量是0.2mol,根据方程式CO+2OH--2e-===CO32-+H2O可知至少消耗标准状况下的CO 2.24 L,故D正确。

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
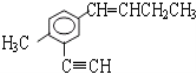
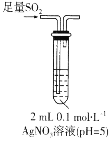
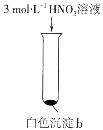
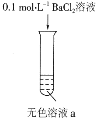
【题目】某实验小组探究SO2与AgNO3溶液的反应,实验记录如下:
序号 | Ⅰ | Ⅱ | Ⅲ |
实验 步骤 |
|
|
|
实验现象 | 得到无色溶液a和白色沉淀b | 产生无色气体,遇空气变为红棕色 | 产生白色沉淀 |
下列说法正确的是
A.透过测Ⅰ中无色溶液a的pH可以判断SO2是否被氧化
B.实验Ⅱ说明白色沉淀b具有还原性
C.实验Ⅲ说明溶液a中一定有![]() 生成
生成
D.实验Ⅰ、Ⅱ、Ⅲ说明SO2与AgNO3溶液反应既有Ag2SO4生成,又有Ag2SO3生成