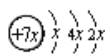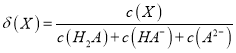题目内容
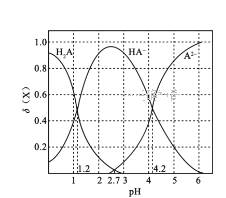
【题目】短周期元素A、B、C、D的位置如右图所示, B、C两元素的原子序数之和是A元素原子序数的4倍,各元素对应的物质相互比较,其中关系正确的是

A.原子半径:C>D>AB.单质的熔点:B>C,D>A
C.最高正价:B>D=A>CD.气态氢化物的稳定性:B>C,D>A
【答案】B
【解析】
设A的质子数设a,则根据元素的位置可知,B、D、C的质子数分别是a+7、a+8、a+9,因此有a+7+a+9=4a,解得a=8,所以A、B、C、D分别是O元素、P元素、Cl元素、S元素。
根据上述分析可知:A是O,B是P,C是Cl,D是S元素。
A. 同一周期元素,从左到右原子半径依次减小,不同周期的元素,原子核外电子层数越多,原子半径越大,则原子半径应该是D>C>A,A错误;
B. 固体单质的熔点高于气体的熔点,则单质的熔点:磷单质>氯气,硫单质>氧气,B正确;
C. 氧元素没有正化合价,C错误;
D. 元素的非金属性越强,其相应的简单的气态氢化物的稳定性就越强,元素的非金属性:Cl>P,O>S,则气态氢化物的稳定性:Cl>P,O>S,D错误;
故合理选项是B。

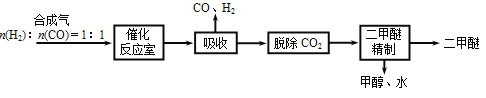
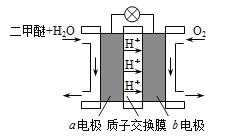
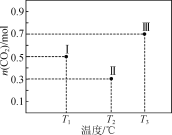
【题目】Ⅰ、某温度下,HNO2和CH3COOH的电离常数分别为5.0×10-4和1.7×10-5。将pH和体积均相同的两种酸溶液分别加水稀释,其pH随加水体积的变化如图所示。
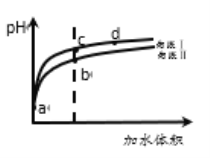
(1)曲线Ⅰ代表____溶液(填“HNO2”或“CH3COOH”,下同)。
(2)a点时,物质的量浓度较大的是______溶液。相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)较少的是_____。
(3)b、c两点溶液中水的电离程度较大的是___ (填“b”或“c”)。
(4)CH3COOH的稀释过程中,下列说法正确的是___ (填编号)。
a.CH3COOH的电离常数增大
b.H+的物质的量减小
c. ![]() 保持不变
保持不变
d. CH3COOH的电离程度增大,溶液的导电能力增强
Ⅱ、25℃,两种酸的电离平衡常数如表。
|
| |
H2A | 4.4×10-7 | 4.7×10-11 |
H2B | 1.3×10-7 | 7.1×10-15 |
(5)HA-的电离平衡常数表达式K =_______。
(6)0.10 molL-1 NaHB溶液中H+、OH-、Na+、HB-的浓度由大到小的顺序为_______。
(7)等浓度的四种溶液:a. Na2A、b. NaHA、c. Na2B、d. NaHB的pH由大到小顺序是_______(填字母)。