题目内容
右图是模拟电化学反应装置图。下列说法正确的是( )
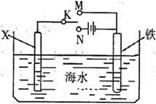

| A.若X为碳棒,开关K置于N处,会加快铁的腐蚀 |
| B.若X为锌,开关K置于N处,则X极上有黄绿色气体生成 |
| C.若X为碳棒,开关K置于M处,则铁电极的电极反应式为:Fe-3e-=Fe3+ |
| D.若X为锌,开关K置于M处,则总反应方程式为:2Zn+O2+2H2O=2Zn(OH)2 |
D
试题分析:选项A、若X为碳棒,开关K置于N处,此时构成的是电解池,铁棒做阴极,发生的是还原反应,故不会加快铁的腐蚀。
选项B、若X为锌,开关K置于N处,此时构成的是电解池,X为阳极,尤其锌为活泼金属,会先参与反应,因此X极上不会有黄绿色气体生成。
选项C、若X为碳棒,开关K置于M处,此时构成的是原电池,X为正极,Y为负极。负极发生氧化反应,其电极反应式为Fe-2e-=Fe2+.故答案为D。
点评:本题综合考查了电解池、原电池的内容,是高考常考内容,属于中等难度题型。解题时,应首先判断所给的装置是原电池还是电解池,其次再根据确定的装置类型进行解答。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目


 ③CH3CH2CH3 ④HC
③CH3CH2CH3 ④HC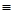 CCH3
CCH3 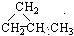 ⑥CH3CH=CHCH3
⑥CH3CH=CHCH3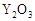 的
的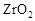 晶体,它在高温下能传导
晶体,它在高温下能传导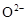 。回答如下问题:①以丁烷(
。回答如下问题:①以丁烷(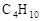 )代表汽油,这个电池放电时发生反应的化学方程式是_________________________________________________________。
)代表汽油,这个电池放电时发生反应的化学方程式是_________________________________________________________。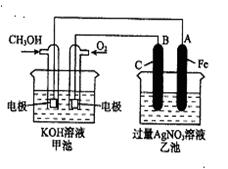

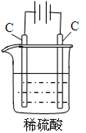
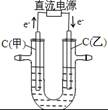

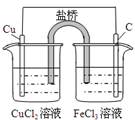
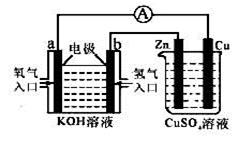
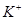 通过,该电池放电时的化学方程式为:
通过,该电池放电时的化学方程式为: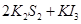 ?=
?=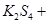 3KI。装置(Ⅱ)为电解示意图,当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是?( )
3KI。装置(Ⅱ)为电解示意图,当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是?( ) 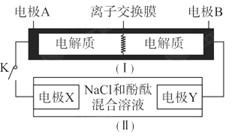
 =
=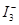
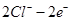 =
=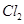 ↑
↑