题目内容
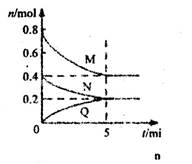
在容积为2 L的恒容的密闭容器中,一定温度下,发生反应:aM(g)+bN(g) cQ(g)。气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述正确的是( )
cQ(g)。气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述正确的是( )
 cQ(g)。气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述正确的是( )
cQ(g)。气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述正确的是( )
| A.该温度下此反应的平衡常数的值K=25/4 |
| B.该反应前5 min的平均速率:v(N)=0.002 mol·L-1·min-1 |
| C.在5 min时,再向体系中充入少量He,重新达到平衡前v(正)>v(逆) |
| D.若开始时向容器中充入2mol M和1mol N,达到平衡时,M的体积分数小于50% |
D
试题分析:A、根据图像可知,平衡时M、N、Q的物质的量分别变化了0.4mol、0.2mol、0.2mol,根据变化量之比是相应的化学计量数之比可知,该反应的化学方程式为2M(g)+N(g)
 Q(g)。平衡时M、N、Q的物质的量浓度分别为0.2mol/L、0.1mol/L、0.1mol/L,所以该温度下平衡常数K=
Q(g)。平衡时M、N、Q的物质的量浓度分别为0.2mol/L、0.1mol/L、0.1mol/L,所以该温度下平衡常数K= =25,A不正确;B、该反应前5 min的平均速率:v(N)=0.1mol/L÷5min=0.02 mol·L-1·min-1,B不正确;C、容器容积不变,则加入He气,物质的浓度不变,因此反应速率不变,平衡不变,C不正确;D、若开始时向容器中充入2mol M和1mol N,则相当于是降低压强,平衡向逆反应方向移动,所以达到平衡时,M的体积分数小于
=25,A不正确;B、该反应前5 min的平均速率:v(N)=0.1mol/L÷5min=0.02 mol·L-1·min-1,B不正确;C、容器容积不变,则加入He气,物质的浓度不变,因此反应速率不变,平衡不变,C不正确;D、若开始时向容器中充入2mol M和1mol N,则相当于是降低压强,平衡向逆反应方向移动,所以达到平衡时,M的体积分数小于 ×100%=50%,D正确,答案选D。
×100%=50%,D正确,答案选D。
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 C(g)在任一时刻的正、逆反应速率可用υ正、υ逆表示:
C(g)在任一时刻的正、逆反应速率可用υ正、υ逆表示:

 2NH3(g) ?H=—92.4kJ?mol?1
2NH3(g) ?H=—92.4kJ?mol?1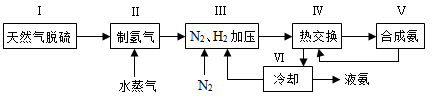
 bZ(g) △H<0。下图是容器中X、Z的物质的量浓度随时间变化的曲线。
bZ(g) △H<0。下图是容器中X、Z的物质的量浓度随时间变化的曲线。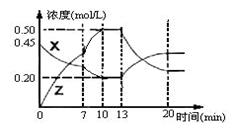
 2NH3,2 min后测得容器中生成了1mol NH3,试求:
2NH3,2 min后测得容器中生成了1mol NH3,试求: 2C(g),?H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500 ℃时充分反应达平衡后C的浓度为ω mol/L,放出热量为b kJ。
2C(g),?H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500 ℃时充分反应达平衡后C的浓度为ω mol/L,放出热量为b kJ。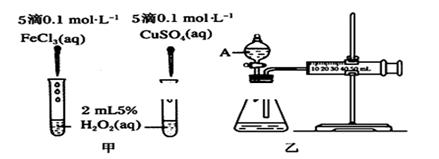

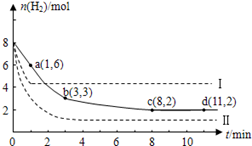
 CH3OH(g)+H2O(g)+49kJ。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标.
CH3OH(g)+H2O(g)+49kJ。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标.