题目内容
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是
| | ①中的物质 | ②中的物质 | 预测①的现象 |
| A | KI溶液 | 浓硝酸 | 溶液变蓝色 |
| B | 酚酞溶液 | 浓氨水 | 无色变红色 |
| C | NaAlO2溶液 | 浓盐酸 | 有白色沉淀 |
| D | 湿润红布条 | 饱和氯水 | 红布条褪色 |
A
解析试题分析:A浓硝酸有挥发性,挥发出的硝酸 溶解在KI溶液中,因它有强的氧化性,将碘离子先氧化为I2,继而再继续氧化为更高的价态,而失去碘水的黄色。故错误。B浓氨水挥发的氨气融入酚酞试液中与水作用得到弱碱-一水合,氨使酚酞变红。正确。C浓盐酸挥发溶解在偏铝酸钠溶液中,与其作用产生氢氧化铝白色沉淀和氯化钠。正确。D饱和氯水挥发的氯气遇湿润红布条时,氯气与水反应产生具有漂白性的次氯酸,而使色布褪色。正确。
考点:考查有挥发性的浓硝酸、浓氨水、浓盐酸及饱和氯水的化学性质。

练习册系列答案
相关题目
下列物质的保存方法正确的是
| A.少量金属钠保存在四氯化碳中 |
| B.氢氧化钠溶液盛放在带有橡胶塞的玻璃试剂瓶中 |
| C.碳酸钠固体保存在细口瓶中 |
| D.白磷保存在干燥的空气中 |
下列物质转化在给定条件下不能实现的是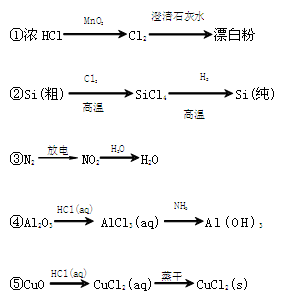
| A.①③⑤ | B.②③④ | C.②③⑤ | D.①④⑤ |
根据下列物质的合理性质,判断其应用不正确的是
| A.Al2O3熔点很高,可用于制作耐高温材料 |
| B.二氧化硅具有半导体性能,可以制成光电池 |
| C.次氯酸钠具有强氧化性,可用于配制消毒液 |
| D.明矾水解产生具有吸附性的胶体粒子,可作漂白剂 |
下列各组物质不能按“→”所示关系实现转化的是(“→”表示反应一步完成)
A. | B. |
C. | D. |
下列各组反应最终有白色沉淀生成的是
①金属钠投入到FeCl2溶液中 ②过量NaOH溶液和AlCl3溶液混合
③少量Ca(OH)2投入NaHCO3溶液中 ④过量CO2通入Na[Al(OH)4]溶液中
| A.②③ | B.③④ | C.①③④ | D.①②③④ |
从绿色化学的理念出发,下列实验不宜用所示装置进行的是( )
| A.不同浓废的硝酸与铜的反应 |
| B.稀硫酸与纯碱或小苏打反应 |
| C.铝与氢氧化钠溶液或稀盐酸反应 |
| D.H2O2在不同催化剂作用下分解 |
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是
| 选项 | W | X |
| A | 盐酸 | Na2CO3溶液 |
| B | NaOH溶液 | AlCl3溶液 |
| C | CO2 | Ca(OH)2溶液 |
| D | Cl2 | Fe |
在某些化学知识用数轴表示能体现出直观形象、简明易记的特点。下列用数轴表示正确的是
A.平衡常数与转化率关系: |
B.Cl2与CH4取代反应后的产物: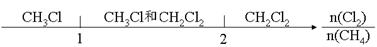 |
C.25℃时,不同pH值的溶液中,水的电离度: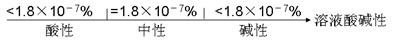 |
D.AlCl3和NaOH反应铝元素的存在形式: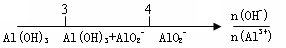 |