题目内容
12.下列物质用途的叙述中,不正确的是( )| A. | 硅可以用作制造太阳能电池 | B. | 二氧化硅可以用于制造光导纤维 | ||
| C. | 石墨可用作绝缘材料 | D. | 石英晶体可用于制造光学仪器 |
分析 A、太阳能电池板的材料是单质硅;
B、光导纤维的主要成分为二氧化硅;
C、石墨能导电;
D、石英晶体有较好的折光率.
解答 解:A、太阳能电池板的材料是单质硅,即硅可以用于制造太阳能电池,故A正确;
B、光导纤维的主要成分为二氧化硅,即二氧化硅能制造光导纤维,故B正确;
C、石墨能导电,是良好的导体,故C错误;
D、石英晶体有较好的折光率,能用于制造光学仪器,故D正确.
故选C.
点评 本题考查了硅和二氧化硅的用途,是高考的高频考点,难度不大,熟记并区分开硅和二氧化硅的用途是关键.

练习册系列答案
相关题目
3.下列离子反应方程式表示正确的是( )
| A. | FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+═4Fe3++2H2O | |
| B. | 过量石灰水与碳酸氢钙反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| C. | 向氯化铝溶液中滴加过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
20.下列各组表述中,两个微粒属于同种元素原子的是( )
| A. | M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p63d64s2 的原子 | |
| B. | 2p能级有一个未成对电子的基态原子和原子的价电子排布为2s22p5 | |
| C. | 3p能级有一个空轨道的基态原子和核外电子的排布为1s22s22p63s23p2 | |
| D. | 最外层电子数是核外电子总数的1/5的原子和价电子排布为4s24p1的原子 |
7.下列离子方程式书写正确的是( )
| A. | 铁与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| B. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| C. | 稀硫酸与氢氧化钡溶液反应:H++OH-═H2O | |
| D. | 铝与氢氧化钠溶液反应:2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑ |
17.据报道,某些花岗岩会产生放射性元素氡(${\;}_{86}^{222}$Rn),下列说法中不正确的是( )
| A. | 该原子的质量数为222 | B. | Rn是86号元素 | ||
| C. | 一个222 86Rn原子中有136个中子 | D. | 一个222 86Rn原子中有136个电子 |
4.下列化学反应能设计成原电池的是( )
| A. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | B. | BaCl2+Na2SO4═2NaCl+BaSO4↓ | ||
| C. | 2NaOH+CO2═Na2CO3+H2O | D. | Zn+CuSO4═ZnSO4+Cu |
1.下列实验装置正确的是( )
| A. |  实验室制乙烯 | B. |  酯化反应 | ||
| C. | 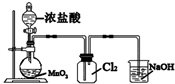 实验室制取Cl2 | D. | 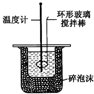 中和热的测定 |
2.“神州八号”飞船成功发射升空之后,完成了与1个月前发射的“天宫一号”的成功交会对接,其中新材料铝锂合金为“太空之吻”提供了保障.下列关于铝锂合金的认识正确的( )
| A. | 铝锂合金是铝与锂形成的一种化合物 | |
| B. | 锂是碱金属元素,性质活泼,铝锂合金与水反应生成氢气 | |
| C. | 铝离子和锂离子的核外电子排布相同 | |
| D. | 若铝锂合金中锂含量为1.1%,则127.3g铝锂合金中含有锂原子0.2mol |
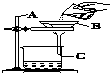 如图所示是某学生设计的过滤操作装置图.
如图所示是某学生设计的过滤操作装置图.