题目内容
在一密闭容器中发生如下反应:,aX(g)+bY(g)?cZ(g);△H>0,下列说法正确的是( )
分析:A.升高温度,正逆反应速率均增大;
B.通入稀有气体使容器体积增大,压强减小,如平衡不移动,则该反应为气体体积不变的反应;
C.体积不变时,密度始终不变;
D.保持容器的体积不变,增加X的量,促进Y的转化.
B.通入稀有气体使容器体积增大,压强减小,如平衡不移动,则该反应为气体体积不变的反应;
C.体积不变时,密度始终不变;
D.保持容器的体积不变,增加X的量,促进Y的转化.
解答:解:A.升高温度,正逆反应速率均增大,正反应为吸热反应,平衡正向移动,故A错误;
B.通入稀有气体使容器体积增大,压强减小,如平衡不移动,则该反应为气体体积不变的反应,则a+b=c,故B正确;
C.体积不变时,密度始终不变,不能判定平衡状态,故C错误;
D.保持容器的体积不变,增加X的量,促进Y的转化,平衡正向移动,但X的转化率减小,故D错误;
故选B.
B.通入稀有气体使容器体积增大,压强减小,如平衡不移动,则该反应为气体体积不变的反应,则a+b=c,故B正确;
C.体积不变时,密度始终不变,不能判定平衡状态,故C错误;
D.保持容器的体积不变,增加X的量,促进Y的转化,平衡正向移动,但X的转化率减小,故D错误;
故选B.
点评:本题考查影响平衡的因素,涉及温度、压强、浓度对平衡的影响及平衡状态的判断,综合性较强,注重基础知识的考查,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
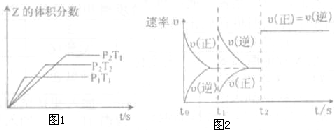 在一密闭容器中发生反应:2X(g)+Y(g)?aZ(g)△H=QkJ?mol-1,开始按体积 比2:1将X、Y充入反应器中,一定条件下发生反应.如图1和图2是根据反应绘制的图象,下列有关说法正确的是( )
在一密闭容器中发生反应:2X(g)+Y(g)?aZ(g)△H=QkJ?mol-1,开始按体积 比2:1将X、Y充入反应器中,一定条件下发生反应.如图1和图2是根据反应绘制的图象,下列有关说法正确的是( )| A、图1,P1>P2,a<3 | B、图1,T1<T2,Q>0 | C、图2,t1时表示恒温、恒压条件下,向平衡体系中充入一定量的Z气体 | D、图2,如果α=3,t2时表示可能向体系中加入了催化剂 |
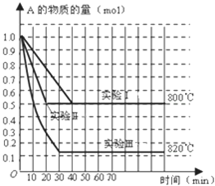 在一密闭容器中发生化学反应:2A(g)?B(g)+C(g);在几种不同条件下进行,其中B、C的起始物质的量为0,反应物A的物质的量随时间变化如图所示,下列说法正确的是( )
在一密闭容器中发生化学反应:2A(g)?B(g)+C(g);在几种不同条件下进行,其中B、C的起始物质的量为0,反应物A的物质的量随时间变化如图所示,下列说法正确的是( )| A、该反应正反应为放热反应 | B、实验Ⅱ和实验Ⅰ比较,实验Ⅱ一定使用了催化剂 | C、在实验Ⅰ中,若容器的体积为0.5L,则从开始到达平衡时间内B的平均反应速率为0.025mol/(L?min) | D、在800℃时,增大压强,若反应重新达平衡时混合气体对氢气的相对密度为64.5,则A的相对分子质量为129 |
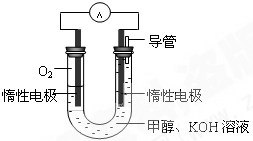 甲醇是重要的化工原料,在日常生活中有着广泛的应用.
甲醇是重要的化工原料,在日常生活中有着广泛的应用. CH3OH(g)△H1
CH3OH(g)△H1 CH3OH(g)+H2O(g)△H2
CH3OH(g)+H2O(g)△H2 已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,E是过渡元素且为地壳中含量较多的金属元素之一.请回答下列问题:
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,E是过渡元素且为地壳中含量较多的金属元素之一.请回答下列问题: