题目内容
铁及其化合物与生产、生活关系密切。
(1)下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
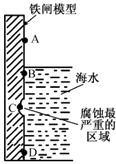
①该电化腐蚀称为 。
②图中A和B区域相比较,腐蚀较慢的是 (填字母)。
(2)实验室经常用到FeCl3溶液,在配制FeCl3溶液时常需加入少量 的 ;将FeCl3溶液和碳酸氢钠溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为 。
(3)已知t℃时,反应FeO(s)+CO(g) Fe( s) +CO2(g)的平衡常数K= 0.25。
Fe( s) +CO2(g)的平衡常数K= 0.25。
①t℃时,反应达到平衡时n(CO2):n(CO)=
②若在1L密闭容器中加人0.02 mol FeO(s),并通入x mol CO,t℃时反应达到平衡。此时
FeO(s)转化率为50%,则x= 。
(1)下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。

①该电化腐蚀称为 。
②图中A和B区域相比较,腐蚀较慢的是 (填字母)。
(2)实验室经常用到FeCl3溶液,在配制FeCl3溶液时常需加入少量 的 ;将FeCl3溶液和碳酸氢钠溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为 。
(3)已知t℃时,反应FeO(s)+CO(g)
 Fe( s) +CO2(g)的平衡常数K= 0.25。
Fe( s) +CO2(g)的平衡常数K= 0.25。①t℃时,反应达到平衡时n(CO2):n(CO)=
②若在1L密闭容器中加人0.02 mol FeO(s),并通入x mol CO,t℃时反应达到平衡。此时
FeO(s)转化率为50%,则x= 。
(1)吸氧腐蚀 A (2) 盐酸  (3)4;1 0.05
(3)4;1 0.05
 (3)4;1 0.05
(3)4;1 0.05试题分析:B中接触了水和氧气,更加容易被腐蚀,制备氯化铁加入盐酸主要是防止氯化铁发生水解。衡常数是指在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值,
但需要注意但是固体和纯液体的浓度视为常数,不能出现在表达式中,
| c(CO2) |
| c(CO) |
则K=
所以n(CO2):n(CO)=1;4
(3)由于FeO(s)转化率为50%即参与反应的FeO为0.01摩尔,则消耗0.01摩尔一氧化碳,生成0.01摩尔的二氧化碳。所以在 平衡时,氧化亚铁的量为0.01、一氧化碳为X-0.01摩尔,二氧化碳为0.01摩尔,据化学平衡常数计算公式可得0.04=X—0.01即X=0.05摩尔

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 2C(气)达到平衡的标志是( )
2C(气)达到平衡的标志是( )  N2O4(g) (无色),如图所示。
N2O4(g) (无色),如图所示。
 2SO3,测得SO3浓度与反应温度关系如图。下列说法正确的是 ( )
2SO3,测得SO3浓度与反应温度关系如图。下列说法正确的是 ( )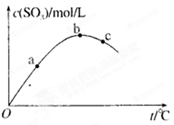
 cZ(g)+dW(g)反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡状态的1.8倍。下列叙述正确的是( )
cZ(g)+dW(g)反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡状态的1.8倍。下列叙述正确的是( )