题目内容
【题目】化学反应速率、化学平衡理论通过大量化学实验进行验证,回答下列相关实验问题。
(1)、Cr2![]() 在溶液中与
在溶液中与![]() 存在一平衡体系,若向体系中加入足量70%的硫酸,溶液呈______色,平衡体系的离子方程式________________________。
存在一平衡体系,若向体系中加入足量70%的硫酸,溶液呈______色,平衡体系的离子方程式________________________。
(2)、探究酸性条件下影响KI溶液被空气氧化的快慢因素,通过观察___________浓度变化比较速率快慢的,KI被氧化的离子方程式___________________。
(3)根据硫代硫酸钠与酸反应探究多种条件对反应速率的影响,下表各组实验中最快出现浑浊的是______;反应离子方程式_________________________________.
Na2S2O3溶液 | 稀H2SO4 | H2O | 温度/℃ | |||
c/mol· | V/mL | c/mol· | V/mL | V/mL | ||
A | 0.1 | 5 | 0.5 | 5 | 10 | 10 |
B | 0.2 | 5 | 0.1 | 5 | 10 | 10 |
C | 0.1 | 5 | 0.1 | 5 | 10 | 30 |
D | 0.2 | 5 | 0.1 | 5 | 10 | 30 |
(4)某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
(实验内容及记录)
实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
0.6 mol/LH2C2O4溶液 | H2O | 0.2 mol/LKMnO4溶液 | 3 mol/L稀硫酸 | ||
1 | 3.0 | V | 3.0 | 2.0 | 4.0 |
2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
请回答:
①根据实验试剂写出实验原理:_____________________(用离子方程式表示)
②分析上述表中的实验数据。V=___mL.实验中加水的目的是________________.
③利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率v(KMnO4)=__________。
【答案】橙色Cr2![]() +H2O
+H2O![]() 2Cr
2Cr![]() +2H+I2或碘4
+2H+I2或碘4![]() +O2+4H+=I2+2H2OD S2
+O2+4H+=I2+2H2OD S2![]() +2H+=S↓+SO2↑+H2O5H2C2O4+2Mn
+2H+=S↓+SO2↑+H2O5H2C2O4+2Mn![]() +6H+=2Mn2++10CO2↑+8H2O2mL确保每次实验c(H2C2O4) c(H2SO4)不变1.5
+6H+=2Mn2++10CO2↑+8H2O2mL确保每次实验c(H2C2O4) c(H2SO4)不变1.5![]() mol·
mol·![]() ·
·![]()
【解析】
(1)加入足量70%的硫酸,氢离子浓度增大,使化学平衡向正反应方向移动,所以溶液由黄色变为橙色;平衡体系的离子方程式为Cr2![]() +H2O
+H2O![]() 2Cr
2Cr![]() +2H+;(2)、探究酸性条件下影响KI溶液被空气氧化的快慢因素,通过观察I2浓度变化比较速率快慢的,KI被氧化生成碘,反应的离子方程式为4
+2H+;(2)、探究酸性条件下影响KI溶液被空气氧化的快慢因素,通过观察I2浓度变化比较速率快慢的,KI被氧化生成碘,反应的离子方程式为4![]() +O2+4H+=I2+2H2O;(3)根据反应浓度越大反应速率越快,反应温度越高反应速率越快,通过表格中数据可知下表各组实验中最快出现浑浊的是D;反应离子方程式为S2
+O2+4H+=I2+2H2O;(3)根据反应浓度越大反应速率越快,反应温度越高反应速率越快,通过表格中数据可知下表各组实验中最快出现浑浊的是D;反应离子方程式为S2![]() +2H+=S↓+SO2↑+H2O;(4)①根据实验试剂为草酸与高锰酸钾反应,故实验原理为:5H2C2O4+2Mn
+2H+=S↓+SO2↑+H2O;(4)①根据实验试剂为草酸与高锰酸钾反应,故实验原理为:5H2C2O4+2Mn![]() +6H+=2Mn2++10CO2↑+8H2O;②分析上述表中的实验数据。V=2mL.实验中加水的目的是确保每次实验c(H2C2O4) 、c(H2SO4)不变;③反应中消耗高锰酸钾的浓度是
+6H+=2Mn2++10CO2↑+8H2O;②分析上述表中的实验数据。V=2mL.实验中加水的目的是确保每次实验c(H2C2O4) 、c(H2SO4)不变;③反应中消耗高锰酸钾的浓度是![]() =0.06mol/L,所以υ(KMnO4)=
=0.06mol/L,所以υ(KMnO4)=![]() =1.5×10-2 mol / (L·min)。
=1.5×10-2 mol / (L·min)。

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案【题目】恒温下,物质的量之比为2∶1的SO2和O2的混合气体在容积为2L的恒容密闭容器中发生反应:2SO2(g)+O2(g) ![]() 2SO3(g) (正反应为放热反应),SO2的物质的量随时间变化的关系如表所示:
2SO3(g) (正反应为放热反应),SO2的物质的量随时间变化的关系如表所示:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
下列说法错误的是
A. 4~5min内,该反应的正、逆反应速率相等
B. 若要提高SO3的产率,则可用过量的空气代替O2
C. 从反应开始到达到平衡,用SO3表示的平均反应速率为0.015mol/ (L·min)
D. 容器内反应达到平衡状态时的压强与起始时的压强之比为5∶4
【题目】中共十九大报告指出,加快水污染防治、实施流域环境和近岸海域综合治理、环境污染的治理是化学工作者研究的重要课题,也是践行“绿水青山就是金山银山”的重要举措。在适当的条件下,将CO2转化为甲醇、甲醚等有机物,既可降低CO2造成的温室效应对环境的影响,还可得到重要的有机产物。
(1)已知:①2H2(g)+O2(g)=2H2O(g) ΔH1=484 kJ/mol
②CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH2=50 kJ/mol
CH3OH(g)+H2O(g) ΔH2=50 kJ/mol
则2CH3OH(g)+3O2(g)= 2CO2(g)+4H2O(g) ΔH,ΔH=_____________。
(2)已知T K时,某恒容密闭容器中存在如下反应:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) ΔH<0,测得容器中不同时刻时各物质的浓度(mol/L)如下表所示:
CH3OCH3(g)+3H2O(g) ΔH<0,测得容器中不同时刻时各物质的浓度(mol/L)如下表所示:
c(CO2) | c(H2) | c(CH3OCH3) | c(H2O) | |
开始时 | a | b | 0 | 0 |
10 s时 | 3 | 0.5 | c | 1.5 |
①若反应开始到10s时间段内,v(H2)=_____________,既能提高反应速率,又能提高H2转化率的方法是________________________。
②若T K时,化学平衡常数K=15,则10 s 时v(正)_______v(逆)(填“>”“<”或“=”),此时CO2的转化率为________。
(3)一定条件下,向某恒容密闭容器中充入x mol CO2和y mol H2,发生的反应为CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=50 kJ·mol1。
CH3OH(g)+H2O(g) ΔH=50 kJ·mol1。
①下图1中能表示该反应的平衡常数K与温度T之间的变化关系曲线为______(填“a”或“b”),其判断依据是__________________________________。
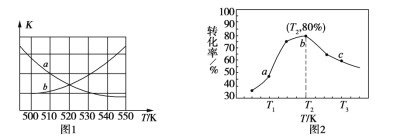
②若x=2、y=3,测得在相同时间内不同温度下H2的转化率如图2所示,则在该时间段内,恰好达到化学平衡时,容器内的压强与反应开始时的压强之比为____________。