题目内容
某化学研究性学习小组探讨Fe3+和SO之间发生怎样的反应,请你一起参与并协助他们完成实验。
(1)提出猜想:
甲同学认为发生氧化还原反应,其反应方程式为___________________________________。
乙同学认为发生了相互促进的水解反应,其反应方程式为:
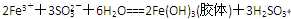 ……
……
(2)实验验证:
丙同学设计了下列实验来探究反应的可能性。
①为了检验所用Na2SO3是否变质,应选用的试剂是________________________________。
②取5 mL FeCl3溶液于试管中,逐滴加入Na2SO3溶液至过量,观察到溶液颜色由黄色变为红褐色(无气泡产生,也无沉淀生成)。
③将②溶液分成两等份,其中一份加入稀盐酸至过量,再加入BaCl2稀溶液,有白色沉淀生成;另一份滴入几滴KSCN溶液,溶液变成血红色。
(3)得出结论:
①根据丙同学的实验得出的结论是:___________________________________。
②实验③中溶液变成血红色的有关离子方程式为___________________________________。
(4)拓展探究:
①丁同学在FeCl3溶液中加入Na2CO3溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是___________________________________。
②从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,两者的水溶液与氯化铁溶液反应的现象差别很大,其可能的原因除 水解能力较
水解能力较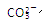 小外,还有___________________________________。
小外,还有___________________________________。
(1)提出猜想:
甲同学认为发生氧化还原反应,其反应方程式为___________________________________。
乙同学认为发生了相互促进的水解反应,其反应方程式为:
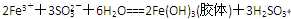 ……
……(2)实验验证:
丙同学设计了下列实验来探究反应的可能性。
①为了检验所用Na2SO3是否变质,应选用的试剂是________________________________。
②取5 mL FeCl3溶液于试管中,逐滴加入Na2SO3溶液至过量,观察到溶液颜色由黄色变为红褐色(无气泡产生,也无沉淀生成)。
③将②溶液分成两等份,其中一份加入稀盐酸至过量,再加入BaCl2稀溶液,有白色沉淀生成;另一份滴入几滴KSCN溶液,溶液变成血红色。
(3)得出结论:
①根据丙同学的实验得出的结论是:___________________________________。
②实验③中溶液变成血红色的有关离子方程式为___________________________________。
(4)拓展探究:
①丁同学在FeCl3溶液中加入Na2CO3溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是___________________________________。
②从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,两者的水溶液与氯化铁溶液反应的现象差别很大,其可能的原因除
 水解能力较
水解能力较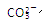 小外,还有___________________________________。
小外,还有___________________________________。(11分)(1)2Fe3++SO32-+H2O=2Fe2++SO42-+2H+(2分)
(2)①BaCl2溶液、稀盐酸(1分)
(3)①Fe3+与SO32-同时发生氧化还原反应和相互促进的水解反应(2分)
②Fe(OH)3(胶体)+3SCN-=Fe(SCN)3+3OH-(2分)
(4)①2Fe3++3 CO32-+3H2O=2Fe(OH)3↓+3CO2↑(2分)
②SO32-有较强的还原性,而CO32-还原性很弱(2分)
(2)①BaCl2溶液、稀盐酸(1分)
(3)①Fe3+与SO32-同时发生氧化还原反应和相互促进的水解反应(2分)
②Fe(OH)3(胶体)+3SCN-=Fe(SCN)3+3OH-(2分)
(4)①2Fe3++3 CO32-+3H2O=2Fe(OH)3↓+3CO2↑(2分)
②SO32-有较强的还原性,而CO32-还原性很弱(2分)
试题分析:(1)铁离子检验氧化性,能把 SO32-氧化生成SO42-,反应的离子方程式是2Fe3++SO32-+H2O=2Fe2++SO42-+2H+.
(2)①如果亚硫酸钠变质,则被氧化生成硫酸钠,所以可以通过检验硫酸钠来检验亚硫酸钠是否变质,即为了检验所用Na2SO3是否变质,应选用的试剂是BaCl2溶液、稀盐酸。
(3)其中一份加入稀盐酸至过量,再加入BaCl2稀溶液,有白色沉淀生成,这说明有硫酸钠生成;另一份滴入几滴KSCN溶液,溶液变成血红色,这说明溶液中还有铁离子,所以Fe3+与SO32-同时发生氧化还原反应和相互促进的水解反应。
(4)①在FeCl3溶液中加入Na2CO3溶液,观察到红褐色沉淀并且产生无色气体,这说明反应中有氢氧化铁和CO2生成,即二者发生的是水解相互促进的反应,所以该反应的离子方程式是2Fe3++3 CO32-+3H2O=2Fe(OH)3↓+3CO2↑。
②由于SO32-有较强的还原性,而CO32-还原性很弱,所以铁离子能和SO32-发生氧化还原反应,而与CO32-不能发生氧化还原反应。
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法。纵观近几年高考,主要以考察探究性实验和物质制备实验为主。这些探究性和制备性实验的试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
 无明显现象
无明显现象 溶液变红
溶液变红 溶液红色未褪去
溶液红色未褪去 溶液明显变黄
溶液明显变黄  溶液变红
溶液变红 溶液变蓝
溶液变蓝 取上层溶液
取上层溶液 溶液变蓝(比试管2中溶液颜色深)
溶液变蓝(比试管2中溶液颜色深)