题目内容
【题目】下列关于溶液和胶体的叙述,正确的是( )
A. 溶液是电中性的,胶体是带电的
B. 通电时,溶液中的溶质粒子不移动,胶体中的分散质粒子向某一极移动
C. 溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D. 一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
【答案】D
【解析】
A、胶体微粒吸附带电离子,带有电荷,但胶体是电中性的,故A错误;B、通电时,溶液中阳离子移向阴极,阴离子移向阳极;胶体微粒移向某一电极发生电泳现象,故B错误;C、溶液中溶质微粒的运动也是无规律的,故C错误;D、一束光线分别通过溶液和胶体时,胶体会出现明显光带,溶液则没有,故D正确;故选D。

【题目】实验室中有一未知浓度的稀盐酸,某同学在实验室中进行实验测定盐酸的浓度。请完成下列填空:
(1)配制100mL0.10molL-1 NaOH标准溶液。
① 主要操作步骤:计算→称量→溶解→_______(冷却后)→洗涤(并将洗涤液移入容量瓶)→定容→摇匀→将配制好的溶液倒入试剂瓶中,贴上标签。
② 称量_____g氢氧化钠固体所需仪器有:天平(带砝码、镊子)、________、烧杯(或表面皿)。
(2)取20.00 mL待测盐酸放入锥形瓶中,并滴加23滴酚酞作指示剂,用配制的标准NaOH溶液进行滴定。重复上述滴定操作23次,记录数据如下:
实验编号 | NaOH溶液的浓度(molL-1) | 滴入NaOH溶液的体积(mL) | 待测盐酸的体积(mL) |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
①碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是________________________________。
②下列试剂①HF溶液 ②KMnO4溶液 ③乙醇 ④CH3COONa溶液,其中_____________(填序号)
不能用酸式滴定管来盛装
③该实验滴定达到终点的标志是_______________________________。
④根据上述数据,可计算出该盐酸的浓度约为_________________(保留两位有效数字)
⑤接近滴定终点时由于滴速过快,如何确定标准液是否滴加过量?_______________________
⑥在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______________________
A.滴定终点读数时俯视读数 B.酸式滴定管使用前,水洗后未用待测盐酸润洗
C.锥形瓶水洗后未干燥 D.碱式滴定管尖嘴部分有气泡,滴定后消失
E.称量NaOH固体时,混入少量KOH杂质
⑦现用以上实验配制的0.10 molL-1NaOH溶液测定食醋中乙酸的浓度,应该选用的试剂为__________
【题目】一定条件下存在反应C(s)+H2O(g)![]() CO(g)+H2(g) ΔH>0,向甲、乙、丙三个恒容容器中加入一定量C 和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
CO(g)+H2(g) ΔH>0,向甲、乙、丙三个恒容容器中加入一定量C 和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
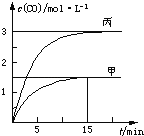
容器 | 甲 | 乙 | 丙 |
容积 | 0.5 L | 0.5 L | V |
温度 | T1℃ | T2℃ | T1℃ |
起始量 | 2 mol C 1 mol H2O | 1 mol CO 1 mol H2 | 4 mol C 2 mol H2O |
A.甲容器中,反应在前15 min的平均速率v(H2)=0.1 mol·L1·min1
B.丙容器的体积V<0.5 L
C.当温度为T1℃时,反应的平衡常数K=2.25
D.乙容器中,若平衡时n(H2O)=0.4 mol,则T1<T2