题目内容
10.把V L含有MgS04和K2S04的混合溶液分成5等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡.则原混合溶液中钾离子的浓度为( )| A. | $\frac{b-2a}{V}$ | B. | $\frac{2b-5a}{V}$ | C. | $\frac{10b-5a}{V}$ | D. | $\frac{5a-10b}{V}$ |
分析 两等份溶液中一份加BaCl2的溶液发生Ba2++SO42-═BaSO4↓,由方程式可知n(SO42-)=n(Ba2+),另一份加氢氧化钠溶液时发生Mg2++2OH-═Mg(OH)2↓,由方程式可知每份溶液中n(Mg2+)=$\frac{1}{2}$n(OH-),再利用电荷守恒可知每份中2n(Mg2+)+n(K+)=2n(SO42-),据此计算每份中n(K+),根据c=$\frac{n}{V}$计算钾离子浓度.
解答 解:混合溶液分成两等份,每份溶液浓度与原溶液浓度相同,
一份加BaCl2的溶液发生Ba2++SO42-═BaSO4↓,由方程式可知n(SO42-)=n(Ba2+)=n(BaCl2)=bmol,
另一份加氢氧化钠溶液时发生Mg2++2OH-═Mg(OH)2↓,由方程式可知每份溶液中n(Mg2+)=$\frac{1}{2}$n(OH-)=$\frac{1}{2}$amol,
由电荷守恒可知每份中2n(Mg2+)+n(K+)=2n(SO42-),故每份中溶液n(K+)=2b-2×$\frac{1}{2}$amol=(2b-a)mol,
则原混合溶液中钾离子的浓度为$\frac{(2b-a)mol}{\frac{1}{5}V}$=$\frac{10b-5a}{V}$mol/L,
故选C.
点评 本题考查混合物反应的计算,为高频考点,题目难度中等,根据电荷守恒计算钾离子的物质的量是关键,试题侧重分析与计算能力的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列实验与物质微粒大小无直接关系的是( )
| A. |  | B. | 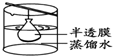 | C. | 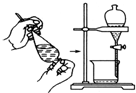 | D. | 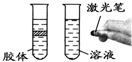 |
5.能用离子方程式H++OH-═H2O表示的化学方程式是( )
| A. | Ba(OH)2+H2SO4═BaSO4↓+2H2O | B. | KOH+HCl═KCl+H2O | ||
| C. | Cu(OH)2+H2SO4═CuSO4+2H2O | D. | 2NaOH+H2S═Na2S+2H2O |
15.关于Fe(OH)3胶体的下列说法中错误的是( )
| A. | 能发生丁达尔效应 | B. | 用FeCl3和烧碱溶液反应制备 | ||
| C. | 微粒直径在1nm-100nm之间 | D. | 能透过滤纸 |
2.同质量的SO2与SO3的说法不正确的是( )
| A. | 分子数目之比为5:4 | B. | 氧原子数目之比为5:6 | ||
| C. | 硫原子数目之比为4:5 | D. | 摩尔质量之比为4:5 |
20.氢氧燃料电池是将H2和O2分别通入电池,穿过浸入20%~40%的KOH溶液的多孔碳电极,其电池反应为2H2+4OH--4e-═4H2O和O2+H2O+4e-═4OH-,则下列叙述正确的是( )
| A. | 通氢气的一极是正极,通氧气的一极是负极 | |
| B. | 通氢气的一极发生的是氧化反应 | |
| C. | 工作一段时间后电解质溶液的pH值增大 | |
| D. | 工作时负极区附近的pH值增大 |
 2NH3(g)△H=+92.4kJ•mol﹣1,下列说法正确的是( )
2NH3(g)△H=+92.4kJ•mol﹣1,下列说法正确的是( )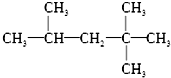 某有机物化合物A的结构简式为:
某有机物化合物A的结构简式为: