题目内容
3.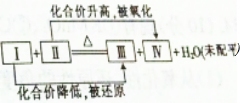 一个化学反应体系中含有浓H2SO4,Cu,H2O,CuSO4,SO2 5种物质,其发生反应的化学方程式可用如图表示,则Ⅳ处的物质是( )
一个化学反应体系中含有浓H2SO4,Cu,H2O,CuSO4,SO2 5种物质,其发生反应的化学方程式可用如图表示,则Ⅳ处的物质是( )| A. | H2SO4 | B. | CuSO4 | C. | Cu | D. | SO2 |
分析 化学反应体系中含有浓H2SO4,Cu,H2O,CuSO4,SO2 5种物质,浓硫酸具有强的氧化性,反应中硫元素化合价降低为二氧化硫,铜具有还原性,能够被浓硫酸氧化生成二价铜离子,据此判断反应物和生成物.
解答 解:化学反应体系中含有浓H2SO4,Cu,H2O,CuSO4,SO2 5种物质,浓硫酸具有强的氧化性,反应中硫元素化合价降低为二氧化硫,铜具有还原性,能够被浓硫酸氧化生成二价铜离子,所以Ⅰ是浓硫酸,Ⅱ是铜,Ⅲ是二氧化硫,Ⅳ是硫酸铜,
故选:B.
点评 本题考查了氧化还原反应,明确氧化还原反应化合价升降规律,明确各物质的性质是解题关键,题目难度不大.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
13.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 1.7g H2O2中含有的电子数为0.9 NA | |
| B. | 等物质的量的N2和CO所含分子数均为NA | |
| C. | 1mol Na2O2 固体中含离子总数为4 NA | |
| D. | 标准状况下,2.24L戊烷所含分子数为0.1 NA |
18.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 16g CH4含有4NA个电子 | |
| B. | 0.1mol铁和0.1mol铜分别与0.1mol氯气完全反应,转移的电子数均为0.2NA | |
| C. | 标准状况下,11.2L H2O中分子数为0.5NA个 | |
| D. | 0.1mol•L-1 Na2CO3溶液中含有0.2NA个Na+ |
8.在温度,容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:[已知2CO(g)+O2(g)?2CO2(g)△H=-566.0KJ/mol-1]
下列关系不正确的是( )
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2mol CO、1mol O2 | 2mol CO2 | 4mol CO2 |
| CO2的浓度(mol•L-1) | C1 | C2 | C3 |
| 反应的能量变化 | 放出aKJ | 吸收bKJ | 吸收CkJ |
| 体系压强(Pa) | P1 | P2 | P3 |
| A. | 2c1<c3 | B. | a+b=283.0 | C. | 2p2>p3 | D. | c1=c2 |
12.列有关Na2C03和NaC03性质的比较中正确的是( )
| A. | 等浓度的溶液中滴入稀盐酸.放出气体的快慢Na2C03<NaC03 | |
| B. | 热稳定性Na2C03<NaHC03 | |
| C. | 常温时水溶性Na2C03<NaHC03 | |
| D. | 相对分子质量Na2C03<NaHC03 |