题目内容
【题目】铝氢化钠(![]() )是有机合成的重要还原剂,其合成线路如下图所示。
)是有机合成的重要还原剂,其合成线路如下图所示。
![]()
(1)无水![]() (
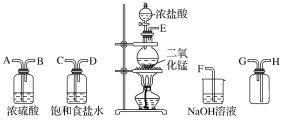
(![]() 升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
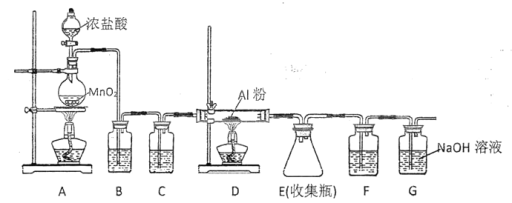
①![]() 中发生反应的化学方程式为__________________。
中发生反应的化学方程式为__________________。
②实验时应先点燃______(填“![]() ”或“
”或“![]() ”)处酒精灯,当观察到____________时,再点燃另一处酒精灯。
”)处酒精灯,当观察到____________时,再点燃另一处酒精灯。
③装置![]() 中盛放饱和NaCl溶液,该装置的主要作用是__________________,请结合方程式进行解释__________________。
中盛放饱和NaCl溶液,该装置的主要作用是__________________,请结合方程式进行解释__________________。
④![]() 中试剂的作用是__________________。用一件仪器装填适当试剂后也可起到
中试剂的作用是__________________。用一件仪器装填适当试剂后也可起到![]() 和
和![]() 的作用,所装填的试剂为__________________。
的作用,所装填的试剂为__________________。
(2)制取铝氢化钠的化学方程式是__________________。
(3)改变![]() 和
和![]() 中的试剂就可以用该装置制取NaH,NaH中氢元素化合价为______,若装置中残留有氧气,制得的NaH中可能含有的杂质为______。
中的试剂就可以用该装置制取NaH,NaH中氢元素化合价为______,若装置中残留有氧气,制得的NaH中可能含有的杂质为______。
(4)铝氢化钠遇水发生剧烈反应,其反应的化学方程式为____________。欲测定铝氢化钠粗产品(只含有NaH杂质)的纯度。称取![]() 样品与水完全反应后,测得气体在标准状况下的体积为
样品与水完全反应后,测得气体在标准状况下的体积为![]() ,样品中铝氢化钠的质量分数为______。(结果保留两位有效数字)
,样品中铝氢化钠的质量分数为______。(结果保留两位有效数字)
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O A 待D中充满黄绿色气体时 除Cl2中混有的HCl Cl2+H2O
MnCl2+Cl2↑+2H2O A 待D中充满黄绿色气体时 除Cl2中混有的HCl Cl2+H2O![]() H++Cl-+HClO饱和氯化钠溶液中氯离子浓度较大,使平衡不容易正移,氯气几乎不溶解,但氯化氢可以溶解,所以可以除杂 防止G中水蒸气进入E使氯化铝水解 碱石灰 AlCl3+4NaH=NaAlH4+3NaCl -1
H++Cl-+HClO饱和氯化钠溶液中氯离子浓度较大,使平衡不容易正移,氯气几乎不溶解,但氯化氢可以溶解,所以可以除杂 防止G中水蒸气进入E使氯化铝水解 碱石灰 AlCl3+4NaH=NaAlH4+3NaCl -1 ![]() NaAlH4+2H2O=NaAlO2+4H2↑ 0.69
NaAlH4+2H2O=NaAlO2+4H2↑ 0.69
【解析】
由实验装置图可知,装置A中二氧化锰和浓盐酸共热制得氯气,用装置B中饱和食盐水除去氯气中混有的氯化氢气体,用装置C中浓硫酸干燥氯气,装置D为氯化铝的制备装置,装置E用于收集氯化铝,用装置F中浓硫酸吸收水蒸气,防止水蒸气进入装置E中,导致氯化铝水解,用装置G中氢氧化钠溶液吸收过量的氯气,防止污染环境。由流程可知,实验制备得到的氯化铝在特定条件下与氢化钠反应制得铝氢化钠。
(1)①装置A中二氧化锰和浓盐酸共热反应生成氯化锰、氯气和水,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
②实验时应先点燃A处酒精灯制备氯气,利用反应生成的氯气排尽装置中的空气,防止空气中氧气干扰实验,待D中充满黄绿色气体时,再点燃D处酒精灯制备氯化铝,故答案为:D中充满黄绿色气体时;
③因浓盐酸具有挥发性,制得的氯气中混有氯化氢,装置B中饱和食盐水的作用是除去氯气中混有的氯化氢气体;选用饱和食盐水的原因是,氯气与水反应为可逆反应,存在如下平衡Cl2+H2O![]() H++Cl-+HClO,饱和氯化钠溶液中氯离子浓度较大,使平衡逆向移动,降低氯气溶解度,使氯气几乎不溶解,但氯化氢极易溶于水,所以可以除杂,故答案为:除
H++Cl-+HClO,饱和氯化钠溶液中氯离子浓度较大,使平衡逆向移动,降低氯气溶解度,使氯气几乎不溶解,但氯化氢极易溶于水,所以可以除杂,故答案为:除![]() 中混有的HCl;Cl2+H2O
中混有的HCl;Cl2+H2O![]() H++Cl-+HClO饱和氯化钠溶液中氯离子浓度较大,使平衡不容易正移,氯气几乎不溶解,但氯化氢可以溶解,所以可以除杂;
H++Cl-+HClO饱和氯化钠溶液中氯离子浓度较大,使平衡不容易正移,氯气几乎不溶解,但氯化氢可以溶解,所以可以除杂;
④F中浓硫酸吸收水蒸气,防止水蒸气进入装置E中,导致氯化铝水解,装置G中氢氧化钠溶液吸收过量的氯气,防止污染环境,若用盛有碱石灰的干燥管代替F和G,可以达到相同的目的,故答案为:防止G中水蒸气进入E使氯化铝水解;碱石灰;
(2)氯化铝在特定条件下与氢化钠反应生成铝氢化钠和氯化钠,反应的化学方程式为AlCl3+4NaH=NaAlH4+3NaCl,故答案为:AlCl3+4NaH=NaAlH4+3NaCl;
(3)若装置A改为氢气的制备装置,D中的钠与氢气共热可以制得氢化钠,由化合价代数和为零可知氢化钠中氢元素为—1价;若装置中残留有氧气,氧气与钠共热会反应生成过氧化钠,故答案为:-1;Na2O2;
(4)铝氢化钠遇水发生剧烈反应生成氢氧化钠和氢气,反应的化学方程式为NaAlH4+2H2O=NaAlO2+4H2↑;氢化钠与水反应的化学方程式为NaH+H2O=NaOH+H2↑,标准状况下22.4L氢气的物质的量为1mol,设铝氢化钠为xmol,氢化钠为ymol,由化学方程式可得联立方程式54x+24y=15.6①4x+y=1②,解得x=y=0.2,,则样品中铝氢化钠的质量分数为![]() ≈0.69,故答案为:NaAlH4+2H2O=NaAlO2+4H2↑;0.69。
≈0.69,故答案为:NaAlH4+2H2O=NaAlO2+4H2↑;0.69。

 名校课堂系列答案
名校课堂系列答案