题目内容
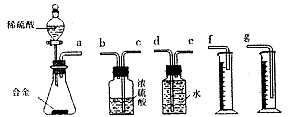
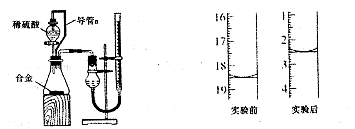
镁铝尖晶石(MgAl2O4)常做耐火材料。共沉淀制备尖晶石的方法是:用AlCl3和MgCl2的混合溶液(用a表示)与过量的氨水(用b表示)反应,再将得到的沉淀高温焙烧。完成下列填空:
(1)为使Mg2+、Al3+同时生成沉淀,应该把 (填“a”或“b”)滴入另一溶液中。
(2)将上述制备反应中部分元素的简单离子:Al3+、Cl–、Mg2+、H+、O2–按半径由大到小的顺序排列
(用离子符号表示)。
(3)AlCl3与氨水反应的反应物和生成物中,属于离子化合物的电子式是 ,属于难溶物的电离方程式 。
(4)不能说明氧元素的非金属性比氮元素强的事实是_________。
a. H2O比NH3稳定 b. 共用电子对偏向:H-O>H-N
c. 沸点:H2O>NH3 d. NO中氮是+2价,氧是-2价
(1)为使Mg2+、Al3+同时生成沉淀,应该把 (填“a”或“b”)滴入另一溶液中。
(2)将上述制备反应中部分元素的简单离子:Al3+、Cl–、Mg2+、H+、O2–按半径由大到小的顺序排列
(用离子符号表示)。
(3)AlCl3与氨水反应的反应物和生成物中,属于离子化合物的电子式是 ,属于难溶物的电离方程式 。
(4)不能说明氧元素的非金属性比氮元素强的事实是_________。
a. H2O比NH3稳定 b. 共用电子对偏向:H-O>H-N
c. 沸点:H2O>NH3 d. NO中氮是+2价,氧是-2价
(1)a(1分)
(2)Cl->O2->Mg2+>Al3+>H+
(3)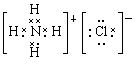 (1分) H++AlO2–+H2O
(1分) H++AlO2–+H2O Al(OH)3
Al(OH)3 Al3++3OH–(2分)
Al3++3OH–(2分)
(4)c(2分)
(2)Cl->O2->Mg2+>Al3+>H+
(3)
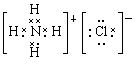 (1分) H++AlO2–+H2O
(1分) H++AlO2–+H2O Al(OH)3
Al(OH)3 Al3++3OH–(2分)
Al3++3OH–(2分) (4)c(2分)
试题分析:(1)为使Mg2+、Al3+同时生成沉淀,应该把AlCl3和MgCl2的混合溶液滴入到过量的氨水中,因此正确的答案选a。
(2)根据微粒电子层越多,半径越大.。在核外电子排布相同的条件下,核电荷数越多,微粒半径越小,据此可知离子的半径大小顺序是Cl->O2->Mg2+>Al3+>H+。
(3)AlCl3与氨水反应生成氢氧化铝沉淀和氯化铵,氯化铵是离子化合物,电子式为
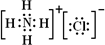 。氢氧化铝是两性氢氧化物,其电离方程式为H++AlO2-+H2O
。氢氧化铝是两性氢氧化物,其电离方程式为H++AlO2-+H2O Al(OH)3
Al(OH)3 Al3++3OH-。
Al3++3OH-。(4)a.非金属性越强,氢化物的稳定性越强,所以根据H2O比NH3稳定,可以证明氧元素的非金属性比氮元素强,故a错误;b.共用电子对偏向:H-O>H-N,证明氧原子的得电子能力强于氮原子,即氧元素的非金属性比氮元素强,故b错误;c.沸点:H2O>NH3是物理性质的表现,但是氧元素的非金属性比氮元素强是化学性质的表现,故C正确;d.NO中氮是+2价,氧是-2价,证明氧原子的得电子能力强于氮原子,即氧元素的非金属性比氮元素强,故d错误,答案选c。

练习册系列答案
相关题目
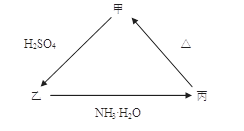
 丙的离子方程式______________________; 丙
丙的离子方程式______________________; 丙 8Cu+4FeO+2Fe2O3+16SO2反应制取铜及其硫和铁的化合物。
8Cu+4FeO+2Fe2O3+16SO2反应制取铜及其硫和铁的化合物。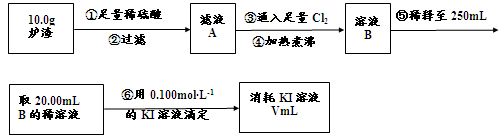
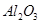 ,含
,含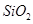 、
、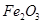 等杂质)中提取氧化铝的工艺做实验,流程如下:
等杂质)中提取氧化铝的工艺做实验,流程如下: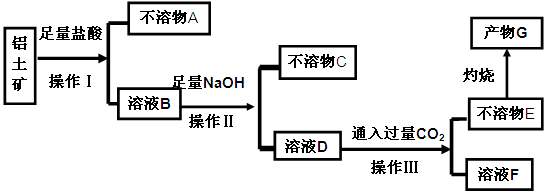
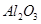 ,含
,含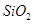 、
、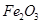 、MgO等杂质)中提取两种工艺品的流程如下:
、MgO等杂质)中提取两种工艺品的流程如下: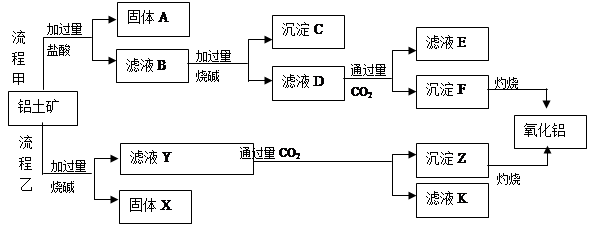
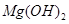 的溶度积常数
的溶度积常数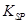 =10-11,取适量的滤液B,加入一定量的烧碱恰使镁离子沉淀完全,则溶液的PH最小为_______.
=10-11,取适量的滤液B,加入一定量的烧碱恰使镁离子沉淀完全,则溶液的PH最小为_______.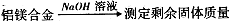 。
。
 。
。