题目内容
【题目】实验小组为验证NO2与水反应的产物,用如图所示装置进行实验(夹持装置已略去,气密性已检验)。
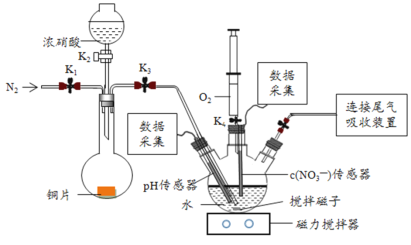
(实验过程)
实验步骤 | 实验现象 |
Ⅰ.打开K1、K3、K5,关闭K2、K4,通入一段时间N2,关闭K1 | —— |
Ⅱ.打开K2,放入足量浓HNO3,同时打开pH传感器和NO3-传感器,记录数据 | 圆底烧瓶中反应剧烈,铜片逐渐溶解,溶液变为蓝绿色, ;片刻后,三颈瓶内的导管口有气泡冒出 |
III.5min后,打开K4,用注射器将少量空气注入三颈瓶,关闭K4 | 三颈瓶内的气体从无色变为浅红棕色 |
步骤II中,传感器记录数据如图所示:
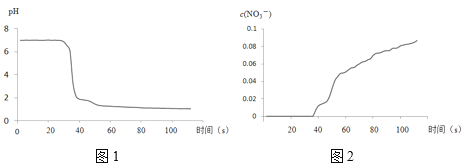
(解释及结论)
(1)NO2与水反应的离子方程式为___。
(2)步骤I中,通入N2的目的是___。
(3)将步骤II中圆底烧瓶内的实验现象补充完整:___。
(4)该实验验证NO2与水反应产物的实验证据包括___(填序号)。
A.圆底烧瓶中溶液变为蓝绿色
B.三颈瓶内的气体从无色变为浅红棕色
C.pH传感器记录所得数据
D.NO3-传感器记录所得数据
(5)有同学认为该实验不严谨,因为也可能导致传感器所记录的数据结果___。
【答案】3NO2+H2O=2H++2NO3-+NO 排出装置中的氧气(空气) 有红棕色气体生成 BCD 圆底烧瓶中浓硝酸的挥发
【解析】
打开K1、K3、K5,关闭K2、K4,通入一段时间N2,排出装置中的氧气(空气);打开K2,放入足量浓HNO3,打开pH传感器和NO3-传感器,铜与浓硝酸发生反应生成硝酸铜、二氧化氮和水;打开K4,用注射器将少量空气注入三颈瓶,三颈瓶内的气体从无色变为浅红棕色的现象可知,二氧化氮与水反应生成一氧化氮和硝酸,生成的一氧化氮被氧气氧化又生成了二氧化氮。
(1)NO2与水反应生成硝酸和一氧化氮,化学反应方程式为:3NO2+H2O=2HNO3+NO,离子反应方程式为:3NO2+H2O=2H++2NO3-+NO,故答案为:3NO2+H2O=2H++2NO3-+NO;
(2)一氧化氮易被空气中的氧气氧化生成二氧化氮,所以通入N2排出装置中的氧气(空气),故答案为:排出装置中的氧气(空气);
(3)步骤II中圆底烧瓶内铜与浓硝酸发生反应生成硝酸铜、二氧化氮和水,所以溶液变为蓝绿色,有红棕色气体生成,故答案为:有红棕色气体生成;
(4)A. 圆底烧瓶中铜与浓硝酸发生反应生成硝酸铜、二氧化氮和水,溶液变为蓝绿色说明生成硝酸铜,不能验证NO2与水反应产物,A错误;
B. 三颈瓶内气体从无色变为浅红棕色,说明一氧化氮与氧气反应生成了二氧化氮,能验证NO2与水反应生成的产物,B正确;
C. pH传感器是用来检测被测物中氢离子浓度并转换成相应的可用输出信号的传感器,随着反应的进行,pH传感器记录所得数据表示,pH减小,酸性增强,能验证NO2与水反应生成的产物,C正确;
D. 随着反应的进行,NO3-传感器记录所得数据表示,NO3-的浓度增大,能验证NO2与水反应生成的产物,D正确;故答案为:BCD;
(5)浓硝酸易挥发,该实验不严谨,有可能导致传感器所记录的数据结构式圆底烧瓶中挥发出来的浓硝酸,故答案为:圆底烧瓶中浓硝酸的挥发。

 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案【题目】碳和碳的化合物在人类生产、生活中的应用非常广泛。“低碳生活”不再只是一种理想,更是一种值得期待的生活方式。
(1)甲烷燃烧时放出大量的热,可作为能源应用于人类的生产和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(1) △H1=-1214.6kJ/mol;
②2CO(g)+O2(g)=2CO2(g) △H2=-566kJ/mol;
则反应CH4(g)+2O2(g)==CO2(g)+2H2O(1)的△H=___。
(2)将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。其负极电极反应式是___。
(3)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
起始量/mol | 平衡量/mol | |||||
实验组 | 温度/℃ | H2O | CO | CO2 | CO | 达到平衡所需时间/min |
1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
①实验1中,以v(H2)表示的平均反应速率为___;
②该反应的正反应为___ (填“吸”或“放”)热反应;
③若要实验3达到与实验2相同的平衡状态(即各物质的体积分数分别相等),则a、b应满足的关系是___(用含a、b的数学式表示)。