题目内容
12.由烃A经下列反应可合成G、H两种不同性能的高聚物塑料.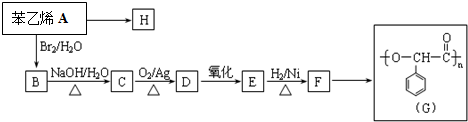
已知C的结构简式为
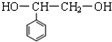 .则:
.则:(1)高聚物H的结构简式是
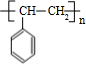 .
.(2)写出下列反应过程的反应类型:
| A→H | A→B | B→C | F→G | |
| 反应类型 |

(4)写出E转化为F的化学方程式
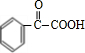 +H2$\stackrel{催化剂}{→}$
+H2$\stackrel{催化剂}{→}$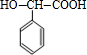 .
.
分析 苯乙烯发生聚合反应生成H,H的结构简式为 ,C的结构简式为
,C的结构简式为  ,可推知,A与溴发生加成反应生成B,故B为
,可推知,A与溴发生加成反应生成B,故B为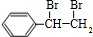 ,B发生水解得C,由G的结构简式可知,F发生缩聚反应生成G,故F为
,B发生水解得C,由G的结构简式可知,F发生缩聚反应生成G,故F为 ,由C的结构及转化关系可知,C氧化得D为
,由C的结构及转化关系可知,C氧化得D为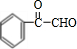 ,D氧化得E为
,D氧化得E为 ,E与氢气发生加成反应得F,据此解答.
,E与氢气发生加成反应得F,据此解答.
解答 解:苯乙烯发生聚合反应生成H,H的结构简式为 ,C的结构简式为
,C的结构简式为  ,可推知,A与溴发生加成反应生成B,故B为
,可推知,A与溴发生加成反应生成B,故B为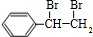 ,B发生水解得C,由G的结构简式可知,F发生缩聚反应生成G,故F为
,B发生水解得C,由G的结构简式可知,F发生缩聚反应生成G,故F为 ,由C的结构及转化关系可知,C氧化得D为
,由C的结构及转化关系可知,C氧化得D为 ,D氧化得E为
,D氧化得E为 ,E与氢气发生加成反应得F,
,E与氢气发生加成反应得F,
(1)由上面的分析可知,H的结构简式为 ,故答案为:
,故答案为: ;
;
(2)由上面的分析可知,反应过程的反应类型:
| A→H | A→B | B→C | F→G | |
| 反应类型 | 加聚反应 | 加成反应 | 取代反应 (或水解反应) | 缩聚反应 |
| A→H | A→B | B→C | F→G | |
| 反应类型 | 加聚反应 | 加成反应 | 取代反应 (或水解反应) | 缩聚反应 |
(3)C氧化得D为
 ,反应的化学方程式为
,反应的化学方程式为 ,
,故答案为:
 ;
; (4)E与氢气发生加成反应得F,反应的化学方程式为
 +H2$\stackrel{催化剂}{→}$
+H2$\stackrel{催化剂}{→}$ ,
,故答案为:
 +H2$\stackrel{催化剂}{→}$
+H2$\stackrel{催化剂}{→}$ .
.点评 本题考查有机物的推断与合成,涉及烯烃、卤代烃、醇、醛、羧酸的性质等,掌握官能团的性质是关键,注意根据题目信息确定含有的官能团,难度中等.

练习册系列答案
相关题目
2.下列反应不属于离子反应的是 ( )
| A. | Ca(OH)2+2HCl═CaCl2+H2O | |
| B. | 2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O | |
| C. | 2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl | |
| D. | Cl2+H2O═HCl+HClO |
3.一种无色气体,可能是由CO2、HBr、NH3、NO2、NO、H2中的一种或几种所组成,将此无色气体通过盛有浓硫酸的洗气瓶,发现气体体积减少,继续通过装有固体Na2O2的干燥管,发现从干燥管出来的气体显红棕色.再将该气体通入盛满水倒立于水槽中的试管内,发现试管内水位上升,最后溶液充满试管.则下列推断不正确的有( )
| A. | 原气体一定含有NH3、NO、CO2 | |
| B. | 原气体一定不含HBr、NO2、H2 | |
| C. | 原气体中NO与CO2的体积比一定为3:2 | |
| D. | 原气体中NO与CO2的体积比一定为2:3 |
20.已知A、B、C、D、E、G都是周期表中前四周期的元素,它们的原子序数依次增大.其中A、C原子的L层有2个未成对电子.D与E同主族,D的二价阳离子与C的阴离子具有相同的电子层结构.G3+离子M层3d轨道电子为半满状态.请根据以上情况,回答下列问题:
(1)写出G基态原子的电子排布式1s22s22p63s23p63d64s2,G位于周期表d区;画出B基态原子外围电子的电子排布图 .
.
(2)A、B、C的第一电离能由小到大的顺序为C<O<N;电负性由小到大的顺序为C<N<O.(用相应的元素符号表示)
(3)G和Mn(质子数为25)两元素的部分电离能数据列于下表:
请回答:
①Mn基态原子的外围电子排布式为3d54s2,核外电子有25种不同的运动状态,占据7种不同能量的原子轨道.
②比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态G2+再失去一个电子难,对此,合理的解释是?Mn2+的3d轨道电子排布为半满状态较稳定,而Fe2+再失去一个电子形成Fe3+的3d轨道电子排布为半满状态较稳定?.
(1)写出G基态原子的电子排布式1s22s22p63s23p63d64s2,G位于周期表d区;画出B基态原子外围电子的电子排布图
 .
.(2)A、B、C的第一电离能由小到大的顺序为C<O<N;电负性由小到大的顺序为C<N<O.(用相应的元素符号表示)
(3)G和Mn(质子数为25)两元素的部分电离能数据列于下表:
| 元素 | Mn | G | |
| 电离能(kJ/mol) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
①Mn基态原子的外围电子排布式为3d54s2,核外电子有25种不同的运动状态,占据7种不同能量的原子轨道.
②比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态G2+再失去一个电子难,对此,合理的解释是?Mn2+的3d轨道电子排布为半满状态较稳定,而Fe2+再失去一个电子形成Fe3+的3d轨道电子排布为半满状态较稳定?.
7.下列实验需要使用温度计的是( )
| A. | 制取溴苯 | B. | 工业乙醇的蒸馏 | C. | 制硝基苯 | D. | 制乙炔 |
2.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.25 NA | |
| B. | 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成56g N2时,转移的电子数目为3.75NA |