题目内容
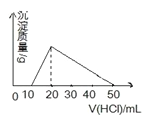
【题目】向100mL 0.1mol/L AlCl3 溶液中,加入c mol/L NaOH 溶液100mL后,再滴加1mol/L 盐酸,滴加盐酸的体积与生成沉淀的质量关系如图所示,则加入的NaOH溶液的浓度为( )
A.0.25mol/L B.0.5 mol/L C.2mol/L D.1mol/L
【答案】B
【解析】
试题分析:分析图像知向100mL 0.1mol/L AlCl3 溶液中加入c mol/L NaOH 溶液100mL所得的混合液中滴加1mol/L 盐酸发生的反应依次为HCl+NaOH=H2O+NaCl、Na[Al(OH)4]+HCl═NaCl+Al(OH)3↓+H2O、Al(OH)3+3HCl═AlCl3+3H2O,沉淀达最大值时,消耗盐酸的体积为20mL,所得溶液为氯化钠溶液,根据电荷守恒知加入NaOH的物质的量为:n(NaOH)=n(Na+)=n(Cl-)=0.1L×0.3mol/L+0.02L×1mol/L
=0.05mol,c(NaOH)=n(NaOH)/V[NaOH(aq)]=0.05mol÷0.1L=0.5mol/L,选B。

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目