题目内容
15.甲、乙、丙均为中学化学常见的不同物质,它们的转化关系如图所示: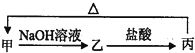
其中甲不可能是( )
| A. | SiO2 | B. | SO2 | C. | NH4Cl | D. | Al2O3 |
分析 A.二氧化硅与氢氧化钠反应生成硅酸钠,硅酸钠与盐酸反应生成硅酸,硅酸分解生成二氧化硅;
B.二氧化硫与与氢氧化钠反应生成亚硫酸钠,亚硫酸钠与少量盐酸反应生成亚硫酸,亚硫酸分解生成二氧化硫;
C.氯化铵与氢氧化钠反应生成氨气,氨气与盐酸反应生成氯化氨;
D.三氧化二铝与氢氧化钠反应生成四羟基合铝酸钠,四羟基合铝酸钠与盐酸反应生成氢氧化铝,氢氧化铝分解生成三氧化二铝.
解答 解:A.若甲二氧化硅,二氧化硅与氢氧化钠反应生成乙硅酸钠,硅酸钠与盐酸反应生成丙硅酸,硅酸分解生成二氧化硅,故A正确;
B.若甲为二氧化硫,二氧化硫与氢氧化钠反应生成亚硫酸钠,亚硫酸钠与与盐酸反应生成亚硫酸,亚硫酸分解分解生成二氧化硫,故B正确;
C.若甲为氯化铵则,氯化铵与氢氧化钠反应生成乙氨气,氨气与盐酸反应生成氯化氨,不符合题意,故C错误;
D.若甲为三氧化二铝,三氧化二铝与氢氧化钠反应生成乙四羟基合铝酸钠,四羟基合铝酸钠与盐酸反应生成丙氢氧化铝,氢氧化铝分解生成三氧化二铝,故D正确;
故选:C.
点评 本题考查了物质转化关系的特征转变、物质性质的应用,主要考查量不同产物不同的常见物质的性质应用,难度中等,等熟悉物质的性质是解题关键.

练习册系列答案
相关题目
5.下列说法正确的是( )
| A. | 2-丁醇发生消去反应产物有2 种 | B. | 卤代烃都能发生水解反应 | ||
| C. | 醇在Cu/△条件下都能氧化成醛 | D. | 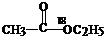 在酸性条件下水解产物是 在酸性条件下水解产物是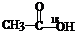 和C2H5OH 和C2H5OH |
6.如图是氢氧燃料电池构造示意图.下列说法不正确的是( )
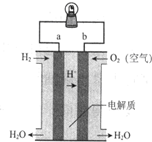

| A. | a极是负极 | B. | 电子由b通过溶液流向a | ||
| C. | 该电池总反应是2H2+O2═H2O | D. | 氢氧燃料电池是环保电池 |
3.下列不能用来鉴别甲烷与乙烯的是( )
| A. | 通入酸性高锰酸钾溶液中 | B. | 通入足量溴水中 | ||
| C. | 一定条件下通入H2 | D. | 点燃 |
10.设NA为阿伏加德罗常数的数值,下列说法正确的是(H-1,O-16)( )
| A. | 标准状况下,22.4 LCCl4含有的分子数为NA | |
| B. | 常温常压下,18g水含有的分子数为 NA | |
| C. | 常温下,1mol Cl2与过量NaOH溶液反应,转移电子总数为2NA | |
| D. | 1L0.1 mol•L-1 Na2CO3溶液中含有CO32-数为0.1 NA |
20.下列说法正确的是( )
| A. | 离子晶体中可能含有共价键,但不一定含有金属元素 | |
| B. | 分子晶体中一定含有共价键 | |
| C. | 非极性分子中一定存在非极性键 | |
| D. | 对于组成和结构相似的分子晶体,一定是相对分子质量越大,熔、沸点越高 |
4.保护环境,就是保护人类自己.目前,在我国的城市环境中最主要的大气污染物是( )
| A. | CO2、Br2、Cl2、酸雨 | B. | NH3、CO2、NO2、雾 | ||
| C. | HCl、SO2、N2、粉尘 | D. | SO2、NO2、CO、烟尘 |
5.下列化学用语正确的是( )
| A. | 硅的原子结构示意图: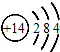 | |
| B. | 原子核内有8个中子的氧原子:${\;}_{8}^{18}$O | |
| C. | 二氧化碳分子的电子式: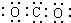 | |
| D. | 甲烷分子的比例模型: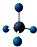 |