题目内容
10.设NA为阿伏加德罗常数的数值,下列说法正确的是(H-1,O-16)( )| A. | 标准状况下,22.4 LCCl4含有的分子数为NA | |
| B. | 常温常压下,18g水含有的分子数为 NA | |
| C. | 常温下,1mol Cl2与过量NaOH溶液反应,转移电子总数为2NA | |
| D. | 1L0.1 mol•L-1 Na2CO3溶液中含有CO32-数为0.1 NA |
分析 A、标况下,四氯化碳为液体;
B、求出水的物质的量,然后根据分子个数N=nNA来计算;
C、氯气与氢氧化钠的反应为歧化反应;
D、CO32-为弱酸根,在溶液中会水解.
解答 解:A、标况下,四氯化碳为液体,故不能根据气体摩尔体积来计算,故A错误;
B、18g水的物质的量为1mol,故含有的水分子个数N=nNA=NA,故B正确;
C、氯气与氢氧化钠的反应为歧化反应,1mol氯气转移1mol电子,即NA个,故C错误;
D、CO32-为弱酸根,在溶液中会水解,故个数小于0.1NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数额有关计算,熟练掌握公式的运用是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列化学用语正确的是( )
| A. | 乙烯分子的最简式:CH2 | B. | 己烷的分子式:C6H12 | ||
| C. | 羟基的化学式:OH- | D. | 1,2-二溴乙烷的结构简式:C2H4Br2 |
1.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1 mol苯分子中含有C=C双键数目为3NA | |
| B. | 标准状况下,11.2 L CCl4中含有的共价键数目为2NA | |
| C. | 1 mol乙烯和乙醇的混合物完全燃烧时消耗O2的分子数为3NA | |
| D. | 常温常压下,17 g 羟基含有的电子总数为10NA |
18.下列反应既是氧化还原反应又是吸热反应的是( )
| A. | Ba(OH)2•8H2O与NH4Cl反应 | |
| B. | 葡萄糖在人体内氧化分解 | |
| C. | 二氧化碳与赤热的碳反应生成一氧化碳 | |
| D. | 锌粒与稀H2SO4反应制取H2 |
5.锌片和纯铜片按图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
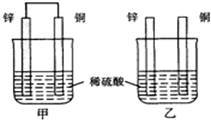

| A. | 两烧杯中溶液的氢离子浓度均减小 | B. | 甲中铜片是正极,乙中铜片是负极 | ||
| C. | 两烧杯中铜片表面均有气泡产生 | D. | 甲、乙溶液均变蓝色 |
15.甲、乙、丙均为中学化学常见的不同物质,它们的转化关系如图所示:
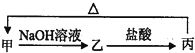
其中甲不可能是( )

其中甲不可能是( )
| A. | SiO2 | B. | SO2 | C. | NH4Cl | D. | Al2O3 |
2.可溶性钡盐有毒,医院中常用硫酸钡这种钡盐作为内服造影剂.医院抢救钡离子中毒患者时,除催吐外,还需要向中毒者胃中灌入硫酸钠溶液.已知:某温度下,Ksp(BaCO3)=5.1×10-9 mol2•L-2;Ksp(BaSO4)=l.1×10-10 mol2•L-2下列推断正确的是( )
| A. | 不用碳酸钡作为内服造影剂,是因为Ksp(BaCO3)>Ksp(BaSO4) | |
| B. | 抢救钡离子中毒患者时,若没有硫酸钠,可以用碳酸钠溶液代替 | |
| C. | 若误饮c(Ba2+)=1.0×10-5 mol•L-1的溶液时,会引起钡离子中毒 | |
| D. | 可以用0.36 mol•L-1的Na2SO4溶液给钡离子中毒患者洗胃 |
19.下列不正确的是( )
| A. | 非金属性:F>O>S | B. | 金属性:Rb>K>Li | ||
| C. | 稳定性:PH3>H2S>HCl | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
20.下列反应属于取代反应的是( )
| A. | 苯与溴水混合后振荡,水层褪色 | |
| B. | 乙烯通入酸性KMnO4溶液中,溶液褪色 | |
| C. | CH4与Cl2的混合气体光照后颜色变浅 | |
| D. | 乙烯通入溴水中,溴水褪色 |