题目内容
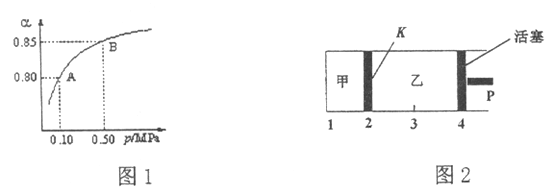
【题目】25℃时,0.1mol Na2CO3与盐酸混合所得溶液的体积为1L,溶液中部分微粒浓度与pH 的关系如图所示。下列有关叙述正确的是

A. 随溶液pH增大,c(CO32-)/c(HCO3-)的值先减小后增大
B. 25℃时,碳酸的第一步电离常数Ka1=10-6
C. pH=4 的溶液中:c(H2CO3)+ c(HCO3-)+ c(CO32-)=0.1mol/L
D. b点所示的溶液中:c(Na+)+c(H+)= 2c(CO32-)+c(OH-)+c(Cl-)
【答案】B
【解析】A. 氢氧根离子能与碳酸氢根离子反应,随溶液pH增大,c(CO32-)/c(HCO3-)的值一直增大,选项A错误;B、25℃时,根据图中信息,当pH=6时,c(H2CO3)= c(HCO3-),碳酸的第一步电离常数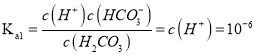 ,选项B正确;C、pH=4,说明反应中有CO2生成,所以根据物料守恒可知c(H2CO3)+c(HCO3-)+c(CO32-)<0.1 molL-1,选项C错误;:D、根据电荷守恒可知,溶液中离子应该满足关系式c(Na+)+c(H+)=2 c(CO32-)+c(OH-)+c(Cl-)+c(HCO3-),选项D错误;答案选B。
,选项B正确;C、pH=4,说明反应中有CO2生成,所以根据物料守恒可知c(H2CO3)+c(HCO3-)+c(CO32-)<0.1 molL-1,选项C错误;:D、根据电荷守恒可知,溶液中离子应该满足关系式c(Na+)+c(H+)=2 c(CO32-)+c(OH-)+c(Cl-)+c(HCO3-),选项D错误;答案选B。

【题目】如表是A、B、C、D、E五种有机物的有关信息:
A | ①能使溴的四氯化碳溶液褪色 ②比例模型为 ③能与水在一定条件下反应生成C |
B | ①由C、H两种元素组成 ②球棍模型为 |
C | ①由C、H、O三种元素组成 ②能与Na反应 ③与E反应生成相对分子质量为88的酯 |
D | ①相对分子质量比C少2 ②能由C催化氧化得到 |
E | ①由C、H、O三种元素组成 ②其水溶液能使紫色石蕊溶液变红 ③可由C发生氧化反应得到 |
回答下列问题:
(1)A~E中,属于烃的是________(填字母)。
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为_______。
(3)C催化氧化生成D的化学方程式为_____________________。
(4)有机物B具有的性质是________(填序号)。
①无色无味的溶液;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色
(5)写出B与溴在催化剂作用下发生反应的化学方程式为_______。
(6)写出E与C反应生成相对分子质量为88的酯的化学方程式为______。