题目内容
【题目】(化学——物质结构与性质)
离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的 EMIM+离子由H、C、N三种元素组成,结构如图所示。回答下列问题:
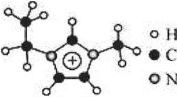
碳原子价层电子的轨道表达式为_____;基态碳原子中,核外电子占据的最高能级的电子云轮廓图为_____形。
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是_____。NH3比PH3的沸点高,原因是______.
(3)氮元素的第一电离能比同周期相邻元素都大的原因是_____。
(4)己知分子中的大![]() 键可用符号
键可用符号![]() 表示,其中n代表参与形成大
表示,其中n代表参与形成大![]() 键的原子数,m代表参与形成大
键的原子数,m代表参与形成大![]() 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大![]() 键可表示为
键可表示为![]() )。EMIM+离子中的五元环跟苯分子相似为平面结构,则EMIM+ 离子中碳原子杂化方式有:_____,其中的大
)。EMIM+离子中的五元环跟苯分子相似为平面结构,则EMIM+ 离子中碳原子杂化方式有:_____,其中的大![]() 键应表示为_____.
键应表示为_____.
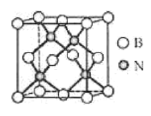
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于晶体,其中硼原子的配位数为_____。已知:立方氮化硼密度为dg/cm3, B原子半径为xpm,N原子半径为xpm,阿伏加德罗常数的值为NA,则该晶胞中原子的空间利用率为______(列出化简后的计算式)。
【答案】![]() 哑铃 NH3 NH3间存在氢键,分子间作用力大于PH3 基态氮原子电子占据的最高能级为半充满,较稳定 sp2、sp3
哑铃 NH3 NH3间存在氢键,分子间作用力大于PH3 基态氮原子电子占据的最高能级为半充满,较稳定 sp2、sp3 ![]() 原子 4
原子 4 ![]() ×100%
×100%
【解析】
(1)碳原子价电子数为4,价电子排布式为2s22p2,所以价层电子的轨道表达式为![]() ;基态碳原子核外电子占据的最高能级为2p,p的电子云轮廓图为哑铃形;
;基态碳原子核外电子占据的最高能级为2p,p的电子云轮廓图为哑铃形;
(2)NH3中N原子价层电子对个数=3+![]() =4,NO3-中N原子价层电子对个数=3+
=4,NO3-中N原子价层电子对个数=3+![]() ;NO2-中N原子价层电子对个数=2+
;NO2-中N原子价层电子对个数=2+![]() ,所以中心原子价层电子对数不同于其他其他两种粒子的是NH3;NH3比PH3的沸点高是因为氨分子间存在氢键;
,所以中心原子价层电子对数不同于其他其他两种粒子的是NH3;NH3比PH3的沸点高是因为氨分子间存在氢键;
(3)VA族比同周期相邻元素都大,是因为最高能级p轨道上电子数为特殊的半充满状态,能量低、较稳定;
(4)根据图1中EMIM+离子中键总数为5个,根据信息,EMIM+离子中C原子的VSEPR模型有四面体和平面三角形两种,即C原子采用sp3、sp2杂化,EMIM+离子有6个电子可形成大π键,可用符号Π56表示;
(5)立方氮化硼硬度仅次于金刚石,晶体类型类似于金刚石,是原子晶体;晶胞中每个N原子连接4个B原子,氮化硼化学式BN,所以晶胞中每个B原子也连接4个N原子,即硼原子的配位数为4;晶胞中N原子数为4,B原子数=8×![]() ,晶胞的质量m=
,晶胞的质量m=![]() ,晶胞的体积V=
,晶胞的体积V=![]() =
=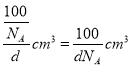 ,B、N原子总体积V’=4×[
,B、N原子总体积V’=4×[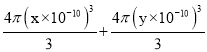 ]=
]=![]() cm3,晶胞中原子的空间利用率=
cm3,晶胞中原子的空间利用率=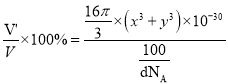 ×100%=
×100%=![]() ×100%。
×100%。
(1)碳原子价电子数为4,价电子排布式为2s22p2,所以价层电子的轨道表达式为![]() ;基态碳原子核外电子占据的最高能级为2p,p的电子云轮廓图为哑铃形;
;基态碳原子核外电子占据的最高能级为2p,p的电子云轮廓图为哑铃形;
(2)NH3中N原子价层电子对个数=3+![]() =4,NO3-
=4,NO3-![]() ;NO2-中N原子价层电子对个数=2+
;NO2-中N原子价层电子对个数=2+![]() ,所以中心原子价层电子对数不同于其他其他两种粒子的是NH3;NH3比PH3的沸点高是因为氨分子间存在氢键;
,所以中心原子价层电子对数不同于其他其他两种粒子的是NH3;NH3比PH3的沸点高是因为氨分子间存在氢键;
(3)VA族比同周期相邻元素都大,是因为最高能级p轨道上电子数为特殊的半充满状态,能量低、较稳定;
(4)根据图1中EMIM+离子中键总数为5个,根据信息,EMIM+离子中C原子的VSEPR模型有四面体和平面三角形两种,即C原子采用sp3、sp2杂化,EMIM+离子有6个电子可形成大π键,可用符号Π56表示,故答案为:sp3、sp2;Π56;
(5)立方氮化硼硬度仅次于金刚石,晶体类型类似于金刚石,是原子晶体;晶胞中每个N原子连接4个B原子,氮化硼化学式BN,所以晶胞中每个B原子也连接4个N原子,即硼原子的配位数为4;晶胞中N原子数为4,B原子数=8×![]() ,晶胞的质量m=
,晶胞的质量m=![]() ,晶胞的体积V=
,晶胞的体积V=![]() =
=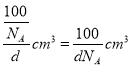 ,B、N原子总体积V’=4×[
,B、N原子总体积V’=4×[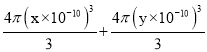 ]=
]=![]() cm3,晶胞中原子的空间利用率=
cm3,晶胞中原子的空间利用率=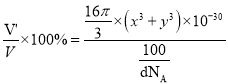 ×100%=
×100%=![]() ×100%。
×100%。

【题目】在潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可用于制取氧气。
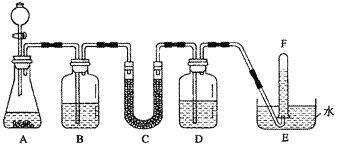
(1)A是用CaCO3制取CO2的装置。写出A中发生反应的化学方程式:
。
(2)按要求填写表中空格:
仪器编号 | 盛放的试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | |
C | 与CO2反应,产生O2 | |
D | 吸收未反应的CO2气体 |
(3)为了达到实验目的, (填“需要”或“不需要”)在B装置之后增加一个吸收水蒸气的装置;若你认为需要增加一个吸收水蒸气装置,应选用 作为吸水剂;若你认为不需要,请说明理由是 。
(4)证明收集到的气体是氧气的方法是 。
【题目】某班几个兴趣小组做了以下实验。
甲组:两同学利用下列试剂:铁粉、0.1mol/L FeCl3溶液、0.1mol/L FeCl2溶液、KSCN溶液、新制氯水,探究Fe2+、Fe3+ 的性质,设计实验方案进行实验,完成下列表格。
探究内容 | 实验方案 | 实验现象 | 写出离子方程式 |
①探究Fe2+具有还原性 | 取少FeCl2溶液,加入少量KSCN溶液后,再往溶液中加入少量________。 | 溶液先不变红,后变为血红色。 | Fe2+发生的反应: _____________ |
②探究Fe3+具有氧化性 | 取少量FeCl3溶液,加入足 量______后,振荡,静置,再往溶液中加入少量KSCN溶液。 | 溶液不变为血红色。 | Fe3+发生的反应:________ |
乙组:两同学利用下图所示的装置进行铁与水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
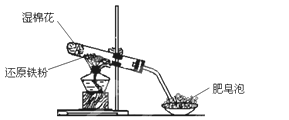
请回答下列问题。
(1)硬质试管中发生反应的化学方程式为_______________。
(2)欲确定反应后硬质试管中固体物质的成分,实验过程如下:
①待硬质试管冷却后,取少许其中的固体物质溶于足量稀硫酸得溶液B;
②取少量溶液B于试管a中,滴加KSCN溶液,溶液没有变红色,则溶液B中的阳离子有_________________,硬质试管中固体物质的成分是_________________。
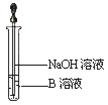
(3)另取少量溶液B,使其与NaOH溶液反应(按图所示),在胶头滴管挤出NaOH溶液的瞬间可观察到生成白色沉淀,沉淀迅速变成灰绿色,最后变成红褐色。请写出与上述现象中白色沉淀转化红褐色沉淀的化学方程式________________。
(4)一段时间后,发现a中未变红的溶液变成红色,原因是 _______________