题目内容
1.下列说法不正确的是( )| A. | SiO2是酸性氧化物,能与NaOH溶液反应 | |
| B. | SiO2不与任何酸反应,可用石英制造耐酸容器 | |
| C. | SiO2是生产光纤制品的基本原料 | |
| D. | 水玻璃可用于生产黏合剂和防火剂 |
分析 根据SiO2的性质:具有酸性氧化物的通性,但SiO2不与水反应,能与HF、NaOH等物质反应来分析.
解答 解:A、因SiO2是酸性氧化物,能与碱反应:SiO2+2NaOH=Na2SiO3+H2O,故A正确;
B、因SiO2 能与氢氟酸反应:SiO2+4HF=SiF4↑+2H2O,故B错误;
C、光导纤维的主要成份是二氧化硅,故C正确;
D、水玻璃是硅酸钠的水溶液,硅酸钠具有黏性,所以可作粘合剂;涂有硅酸钠溶液的木条加热时,水分蒸发后不易燃烧,所以可作防火剂,故D正确;
故选:B.
点评 本题主要考查了SiO2的化学性质,需要强调的是SiO2作为酸性氧化物,但也不完全具有酸性氧化物的通性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.在无色透明的强酸性溶液中,能大量共存的离子组是( )
| A. | K+、Ba2+、NO3-、SO42- | B. | K+、Na+、Cl-、ClO- | ||
| C. | Ca2+、NH4+、NO3-、Cl- | D. | K+、Na+、MnO4-、SO42- |
12.设NA为阿伏伽德罗常数的值.下列说正确的是( )
| A. | 高温下,0.2molFe与足量稀硫酸反应反应,生成的H2分子数目为0.3NA | |
| B. | 2 L0.5 mol×L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | C2H4和N2组成的42g混合气体中原子的个数为3NA | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28gN2 时,转移的电子数目为3.75NA |
9.下列说法正确的是( )
| A. | BaSO4不溶于水,其水溶液导电能力弱,因此BaSO4是非电解质 | |
| B. | 168O、178O、188O互为同位素原子,它们的化学性质完全不同 | |
| C. | 元素的化合价与其在反应中失去或得到电子的数目存在一定的关系 | |
| D. | CO2的水溶液能导电,因此CO2是电解质 |
6.下列元素中,属于第三周期的是( )
| A. | K | B. | P | C. | F | D. | N |
13.${\;}_{6}^{13}C$呼气法在医学上常用于门螺旋杆菌的诊断,下列关于${\;}_{6}^{13}C$的说法中正确的是( )
| A. | 质子数是6 | B. | 质量数是6 | C. | 电子数是13 | D. | 中子数是13 |
10.下列条件一定能使化学反应速率增大的是( )
①增加反应物的量 ②升高温度 ③缩小反应容器的体积 ④加入生成物.
①增加反应物的量 ②升高温度 ③缩小反应容器的体积 ④加入生成物.
| A. | 只有② | B. | 只有②③ | C. | 只有①② | D. | 全部 |

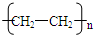 ,反应类型为加聚反应.
,反应类型为加聚反应.