题目内容
12.设NA为阿伏伽德罗常数的值.下列说正确的是( )| A. | 高温下,0.2molFe与足量稀硫酸反应反应,生成的H2分子数目为0.3NA | |
| B. | 2 L0.5 mol×L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | C2H4和N2组成的42g混合气体中原子的个数为3NA | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28gN2 时,转移的电子数目为3.75NA |
分析 A、铁与稀硫酸反应后变为+2价;
B、1mol硫酸根带电荷数为2mol;
C、C2H4和N2的摩尔质量均为28g/mol;
D、此反应转移15mol电子.
解答 解:A、铁与稀硫酸反应后变为+2价,故0.2mol铁失去0.4mol电子,生成0.2mol氢气,故A错误;
B、1mol硫酸根带电荷数为2mol,2 L0.5 mol×L-1硫酸钾溶液中硫酸根为2L×0.5mol/L=1mol,带电荷数为2mol,故B错误;
C、C2H4和N2的摩尔质量均为28g/mol,故42g混合气体的物质的量为1.5mol,而1molC2H4和N2含有的原子的物质的量分别为6mol和2mol,故1.5mol混合气体中含有的原子的物质的量介于9mol到3mol之间,故C错误;
D、此反应转移15mol电子时生成4mol氮气,故当生成28g氮气即1mol氮气时,转移的电子的物质的量为3.75mol,故D正确.故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
2.设NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 22.4LCl2中含有NA个Cl2分子 | |
| B. | 1L 0.1mol.L-1Na2SO4溶液中有0.1NA个Na+ | |
| C. | 从1L1mol.L-1的NaCl溶液中取出10mL,其物质的量浓度为0.01mol.L-1 | |
| D. | 1molCa变成Ca2+时失去的电子数为2NA |
3.在温度t1和t2下,X2(g)和 H2反应生成HX的平衡常数如表:
(1)已知t2>t1,HX的生成反应是放热反应(填“吸热”或“放热”).
(2)HX的电子式是 .
.
(3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是HF>HCl>HBr>HI.
(4)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,ad.
a.在相同条件下,平衡时X2的转化率逐渐降低
b.X2与H2反应的剧烈程度逐渐减弱
c.HX的还原性逐渐减弱
d.HX的稳定性逐渐减弱.
| 化学方程式 | K (t1) | K (t2) |
| F2+H2?2HF | 1.8×1036 | 1.9×1032 |
| Cl2+H2?2HCl | 9.7×1012 | 4.2×1011 |
| Br2+H2?2HBr | 5.6×107 | 9.3×106 |
| I2+H2?2HI | 43 | 34 |
(2)HX的电子式是
 .
.(3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是HF>HCl>HBr>HI.
(4)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,ad.
a.在相同条件下,平衡时X2的转化率逐渐降低
b.X2与H2反应的剧烈程度逐渐减弱
c.HX的还原性逐渐减弱
d.HX的稳定性逐渐减弱.
20.由乙烯推测丙烯(CH2=CH-CH3)的结构或性质,下列说法中不正确的是( )
| A. | 丙烯分子中所有原子都在同一平面上 | |
| B. | 丙烯可使酸性高锰酸钾溶液褪色 | |
| C. | 丙烯可使溴水褪色 | |
| D. | 丙烯能发生加成反应 |
7.在下列反应中,盐酸既表现还原性又表现酸性的是( )
| A. | NaOH+HCl═NaCl+H2O | B. | MnO2+4HCl(浓)═MnCl2+2H2O+Cl2↑ | ||
| C. | Fe+2HCl═FeCl2+H2↑ | D. | CaCO3+2HCl═CaCl2+H2O+CO2↑ |
17.以下课堂实验中对实验现象描述正确的是( )
| A. | 铁丝在氯气中燃烧,放出大量的热,生成白色烟雾 | |
| B. | 氢气在氯气中安静地燃烧,火焰呈浅蓝色,瓶口有白雾产生 | |
| C. | 已吸入氯气的针筒中吸入氢氧化钠溶液,针筒内的气体体积迅速变小,黄绿色立即褪去 | |
| D. | 在充满氯气的集气瓶中放入干燥的红色纸片,红色消失 |
4.电解质溶液有许多奇妙之处,你只有深入思考,才能体会到它的乐趣.下列关于电解质溶液的叙述中正确的是( )
| A. | Na2CO3、NaHCO3两种盐溶液中,离子种类不相同 | |
| B. | 常温下,1 mol•L-1的CH3COOH溶液与1 mol•L-1的NaOH溶液等体积混合后,所得混合液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | 物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c(NH4+)前者小于后者 | |
| D. | 常温下,某溶液中由水电离出的c(H+)=10-5 mol•L-1,则此溶液可能是盐酸 |
1.下列说法不正确的是( )
| A. | SiO2是酸性氧化物,能与NaOH溶液反应 | |
| B. | SiO2不与任何酸反应,可用石英制造耐酸容器 | |
| C. | SiO2是生产光纤制品的基本原料 | |
| D. | 水玻璃可用于生产黏合剂和防火剂 |
 写出有关反应方程式
写出有关反应方程式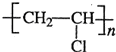
 .
.