题目内容
9.下列叙述正确的是( )| A. | 元素处于最高价态,一定具有最强的氧化性 | |
| B. | 阳离子只有氧化性,阴离子只有还原性 | |
| C. | 还原剂失电子越多,还原性越强 | |
| D. | 在化学反应中,某元素由化合态变为游离态,此元素可能被氧化,也可能被还原 |
分析 A.元素处于最高价态,不一定具有最强的氧化性;
B.阳离子可能具有还原性,阴离子也可能具有氧化性;
C.还原性的强弱决定于失电子能力的强弱;
D.元素从化合态到游离态,根据其化合态时的价态分析.
解答 解:A.元素处于最高价态,不一定具有最强的氧化性,例如Na +,故A错误;
B.阳离子可能具有还原性,如Fe 2+,阴离子也可能具有氧化性,如 MnO4-,故B错误;
C.还原性的强弱决定于失电子能力的强弱,与失电子的多少无关,故C错误;
D.因为元素从化合态到游离态,既有可能被氧化又有可能被还原,须看其化合态时的价态:正价→0价,被还原,负价→0价,被氧化,故D正确.
故选:D.
点评 本题考查了氧化还原反应,题目难度不大,注意把握物质氧化性、还原性与化合价的关系.

练习册系列答案
相关题目
19.下列叙述正确的是( )
| A. | 粗铜提纯时以硫酸铜溶液作电解液,精铜作阳极 | |
| B. | 铁钉镀铜时铁钉做阴极,发生氧化反应 | |
| C. | 用惰性电极电解CuSO4溶液一段时间后再加入纯净的CuO,可以使溶液恢复到原来的成分和浓度 | |
| D. | 粗铜提纯时电解后Fe、Zn、Ag等杂质会沉积在电解槽底部形成阳极泥 |
17.用惰性电极电解Fe2(SO4)3和CuSO4的混合溶液,下列说法正确的是( )
| A. | 阴极反应式为:Cu2++2e-═Cu,当有Cu2+存在时,Fe3+不放电 | |
| B. | 阴极上首先析出铁,然后析出铜 | |
| C. | 阴极先是Fe3+放电,后Cu2+放电 | |
| D. | 阴极上不可能析出铜 |
4.SO2通过下列工艺流程可制得化工业原料H2SO4和清洁能源H2.
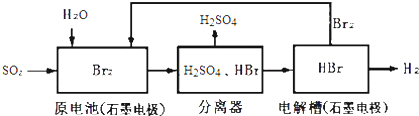
(1)根据资料:
为检验分离器的分离效果,取分离后的H2SO4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到无淡黄色沉淀产生,最终生成白色沉淀,证明分离效果较好.
(2)表示该工艺流程的总反应化学方程式为:SO2+2H2O=H2SO4+H2;该生产工艺的优点有溴可以循环利用,获得清洁能源氢气(答一点即可).
(3)某含有大量氯化银沉淀的悬浊液中c(Cl-)=0.36mol•L-1,加入等体积的溴化钠溶液,若要产生溴化银沉淀,加入的溴化钠溶液的最小浓度是10-3mol•L-1.

(1)根据资料:
| 化学式 | Ag2SO4 | AgBr | AgCl |
| Ksp | 1.4×10-5 | 5.0×10-13 | 1.8×10-10 |
(2)表示该工艺流程的总反应化学方程式为:SO2+2H2O=H2SO4+H2;该生产工艺的优点有溴可以循环利用,获得清洁能源氢气(答一点即可).
(3)某含有大量氯化银沉淀的悬浊液中c(Cl-)=0.36mol•L-1,加入等体积的溴化钠溶液,若要产生溴化银沉淀,加入的溴化钠溶液的最小浓度是10-3mol•L-1.
14.2015年6月5日世界“环境日”中国的主题是“践行绿色生活”.下列不符合这一主题的是( )
| A. | 从自身做起,从身边小事做起,减少超前消费、炫耀性消费、奢侈性消费和铺张浪费现象 | |
| B. | 减少温室气体的排放,倡导“绿色低碳”的生活 | |
| C. | 少开私家车,提倡“绿色出行” | |
| D. | 向空气中喷洒烧碱溶液,避免酸雨的发生 |
1.甲、乙两烧杯中分别盛有100mL 3mol/L的硫酸和NaOH溶液,向两烧杯中各加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=2:3,则加入铝粉的质量为( )
| A. | 5.4g | B. | 7.2g | C. | 8.1g | D. | 10.8g |
18.下列叙述中错误的是( )
| A. | 原子半径 Na>Si>Cl | B. | 金属性 Na>Mg>Al | ||
| C. | 稳定性 SiH4<HCl<H2S | D. | 酸性 H3PO4<H2SO4<HClO4 |
19.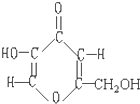 曲酸是一种非常有潜力的食品添加剂.经测定曲酸的分子式为C6H6O4,结构式如图所示,试根据曲酸分子结构特点,推测曲酸不可能具有的性质为( )
曲酸是一种非常有潜力的食品添加剂.经测定曲酸的分子式为C6H6O4,结构式如图所示,试根据曲酸分子结构特点,推测曲酸不可能具有的性质为( )
 曲酸是一种非常有潜力的食品添加剂.经测定曲酸的分子式为C6H6O4,结构式如图所示,试根据曲酸分子结构特点,推测曲酸不可能具有的性质为( )
曲酸是一种非常有潜力的食品添加剂.经测定曲酸的分子式为C6H6O4,结构式如图所示,试根据曲酸分子结构特点,推测曲酸不可能具有的性质为( )| A. | 能发生酯化反应 | B. | 易溶于水、醇 | C. | 具有抗氧化性 | D. | 具有强酸性 |