题目内容
F2和Xe在一定条件下可生成XeF2、XeF4和 XeF6三种氟化氙,它们都是极强的氧化剂,下列关于Xe的氟化物的叙述不正确的是( )
分析:A.Xe原子的最外层电子数为8;
B.三种氟化氙的构成微粒均为分子;
C.相对分子质量越大,熔点越大;
D.Xe位于零族,与He同族.
B.三种氟化氙的构成微粒均为分子;
C.相对分子质量越大,熔点越大;
D.Xe位于零族,与He同族.
解答:解:A.Xe原子的最外层电子数为8,则XeF2分子中Xe原子最外层不是八电子结构,多于8个电子,故A正确;
B.XeF2、XeF4和XeF6的构成微粒均为分子,则固体均为分子晶体,故B正确;
C.分子晶体的相对分子质量越大,熔点越大,则熔点大小顺序XeF2<XeF4<XeF6,故C正确;
D.Xe元素的所在族的原子(He除外)的外围电子排布式均为ns2np6,He的外围电子为1s2,均为非金属元素,故D错误;
故选D.
B.XeF2、XeF4和XeF6的构成微粒均为分子,则固体均为分子晶体,故B正确;
C.分子晶体的相对分子质量越大,熔点越大,则熔点大小顺序XeF2<XeF4<XeF6,故C正确;
D.Xe元素的所在族的原子(He除外)的外围电子排布式均为ns2np6,He的外围电子为1s2,均为非金属元素,故D错误;
故选D.
点评:本题属于信息习题,以信息的方式考查电子排布、分子晶体熔点的比较等,注意结合所学知识来解答,题目难度不大.

练习册系列答案
相关题目
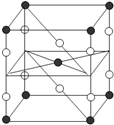 F2和Xe在一定条件下可生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂(其氧化性依次递增),都极易水解,其中:6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑下列推测正确的是( )
F2和Xe在一定条件下可生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂(其氧化性依次递增),都极易水解,其中:6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑下列推测正确的是( )| A、XeF2分子中各原子均达到八电子结构 | B、某种氟化氙的晶体结构单元如右图,可推知其化学式为XeF6 | C、XeF4按已知方式水解,每生成4molXe,转移16mol电子 | D、XeF2加入水中,在水分子作用下将重新生成Xe和F2 |