题目内容
17. 分子式为C3H7Br的有机物甲在适宜的条件下能发生如下一系列转化:
分子式为C3H7Br的有机物甲在适宜的条件下能发生如下一系列转化:(1)若B能发生银镜反应,试回答下列问题:
①试确定有机物甲的结构简式:CH3CH2CH2Br
②用化学方程式表示下列转化过程:
甲+NaOH水溶液:CH3CH2CH2Br+NaOH$→_{△}^{H_{2}O}$CH3CH2CH2OH+NaBr;
B+Ag(NH3)2OH:CH3CH2CHO+2Ag(NH3)2OH$\stackrel{水浴加热}{→}$CH3CH2COONH4+3NH3+2Ag↓+H2O.
(2)若B不能发生银镜反应,请用化学方程式表示下列转化过程:A→B2CH3CH(OH)CH3+O2$→_{△}^{Cu}$2CH3COCH3+2H2O;C→D
 .
.
分析 (1)若B能发生银镜反应,则说明甲的水解产物A中-OH所在的碳原子上有2个氢原子,则A为1-丙醇,即甲为1-溴丙烷,B为丙醛,C为1-丙醇的消去产物,为丙烯,D为聚丙烯;
(2)若B不能发生银镜反应,则说明甲的水解产物A中-OH所在的碳原子上只有1个氢原子,则A为2-丙醇,即甲为2-溴丙烷,B为丙酮,C为2-丙醇的消去产物,为丙烯,D为聚丙烯.
解答 解:(1)若B能发生银镜反应,则说明甲的水解产物A中-OH所在的碳原子上有2个氢原子,则A为1-丙醇,即甲为1-溴丙烷,B为丙醛,C为1-丙醇的消去产物,为丙烯,D为聚丙烯.
①由以上分析可知甲为1-溴丙烷,为CH3CH2CH2Br,故答案为:CH3CH2CH2Br;
②甲转化为C,是1-溴丙烷发生卤代烃的消去反应,故化学方程式为CH3CH2CH2Br+NaOH$→_{△}^{H_{2}O}$CH3CH2CH2OH+NaBr,
B为丙醛,能和银氨溶液Ag(NH3)2OH发生银镜反应,化学方程式为CH3CH2CHO+2Ag(NH3)2OH$\stackrel{水浴加热}{→}$CH3CH2COONH4+3NH3+2Ag↓+H2O,
故答案为:CH3CH2CH2Br+NaOH$→_{△}^{H_{2}O}$CH3CH2CH2OH+NaBr;CH3CH2CHO+2Ag(NH3)2OH$\stackrel{水浴加热}{→}$CH3CH2COONH4+3NH3+2Ag↓+H2O;
(2)若B不能发生银镜反应,则说明甲的水解产物A中-OH所在的碳原子上只有1个氢原子,则A为2-丙醇,即甲为2-溴丙烷,B为丙酮,C为2-丙醇的消去产物,为丙烯,D为聚丙烯,
A转化为B为醇的催化氧化,化学方程式为:2CH3CH(OH)CH3+O2$→_{△}^{Cu}$2CH3COCH3+2H2O,C为丙烯,发生加聚反应生成聚丙烯,方程式为 ,
,
故答案为:2CH3CH(OH)CH3+O2$→_{△}^{Cu}$2CH3COCH3+2H2O; .
.
点评 本题考查了有机物的推断,以B为突破口采用正逆相结合的方法进行分析推断,明确有机物的官能团及其性质结合反应条件即可解答,注意卤代烃中卤元素检验方法,难度中等.

 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案①混合气体的总分子数不再变化
②混合气体的颜色不再变化
③容器的总压强不再变化
④混合气体的总质量不再变化
⑤混合气体的密度不再变化
⑥单位时间内生成nmol的NO,同时消耗nmol的NO2.
| A. | ①②③ | B. | ④⑤⑥ | C. | ①②④ | D. | ③⑤⑥ |
| A. | 50mL 1.5mol•L-1的CaCl2溶液 | B. | 100mL 3mol•L-1的NH4Cl溶液 | ||
| C. | 75mL 3mol•L-1的KCl溶液 | D. | 50mL 2mol•L-1的FeCl2溶液 |
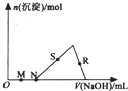 向HC1、AlCl3混合溶液中逐滴加入NaOH溶液,生成沉淀的量随NaOH溶液加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是( )
向HC1、AlCl3混合溶液中逐滴加入NaOH溶液,生成沉淀的量随NaOH溶液加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是( )| A. | M点对应的溶液中:K+、Fe2+、SO42-、NO3- | |
| B. | N点对应的溶液中:K+、NH4+、Cl-、CO32- | |
| C. | S点对应的溶液中:Na+、SO42-、HCO3-、NO3- | |
| D. | R点对应的溶液中:Na+、SO42-、Cl-、NO3- |