题目内容
1.关于化学键的各种叙述中,下列说法中正确的是( )| A. | 在离子晶体里,只存在离子键 | |
| B. | 共价化合物里,一定不存在离子键 | |
| C. | 非金属元素之间只能形成共价键 | |
| D. | 由不同种元素组成的多原子分子里,一定只有极性键 |
分析 A.含有离子键的化合物为离子化合物;
B.只含共价键的化合物为共价化合物;
C.氯化铵为非金属元素组成的离子化合物;
D.由不同种元素组成的多原子分子里,可能存在非极性键.
解答 解:A.在离子化合物中,一定含有离子键,可以含有共价键,例如氢氧化钠,故A错误;
B.只含共价键的化合物为共价化合物,所以共价化合物里,一定不存在离子键,故B正确;
C.非金属元素之间可以形成离子化合物,例如氯化铵,故C错误;
D.由不同种元素组成的多原子分子里,可能存在非极性键,如H2O2中存在O-O非极性键,故D错误;
故选:B.
点评 本题考查了物质和化学键的关系,明确共价化合物、离子化合物的概念即可解答,题目难度不大.

练习册系列答案
相关题目
6.用下列实验装置进行的相关实验,设计合理且能达到相应实验目的是 ( )
| A. |  装置:石油的分馏 | |
| B. |  装置:测定中和热 | |
| C. | 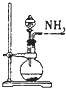 装置:将浓氨水滴加到生石灰中制取氨气 | |
| D. |  装置:加热氯化铵和消石灰混合物,制取并收集氨气 |
12.下列叙述中能肯定A金属比B金属活泼性强的是( )
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | A原子的电子层数比B原子的电子层数多 | |
| C. | 1mol A从酸中置换H+生成的H2比1mol B从酸中置换H+生成的H2多 | |
| D. | 常温时,A能从水中置换出氢,而B不能 |
9.现有某化学式为C3H6O3的有机物,其1H核磁共振谱有三个峰,强度之比为3:2:1,则该有机物的结构简式不可能为( )
| A. | CH3CH2COOH | B. | HCOOCH2CH3 | C. | CH3COOCH3 | D. | CH3COCH2OH |
13.在检验SO42-的过程中,下列操作中正确的是( )
| A. | 先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有SO42-存在 | |
| B. | 先加入硝酸钡,产生白色沉淀,然后再加稀硝酸,沉淀不溶解,证明有SO42-存在 | |
| C. | 先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO42-存在 | |
| D. | 先加入氯化钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO42-存 |
10.下列指定粒子的个数比不为2:1的是( )
| A. | Be2+中的质子数和电子数比 | |
| B. | ${\;}_{1}^{3}$H原子中的中子数和电子数 | |
| C. | Na2CO3晶体中阳离子和阴离子个数比 | |
| D. | BaO2(过氧化钡)固体中阴离子和阳离子个数比 |
 .
.