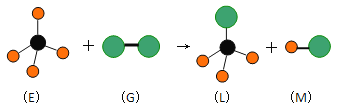
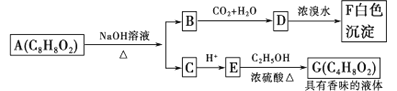
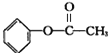
题目内容
【题目】某研究性学习小组将下列装置按如图连接,C、D、E、F、X、Y都是惰性电极,甲、乙、丙 中电解质溶液含溶质均为 1 mol。将电源接通后,向乙中滴入酚酞溶液,在 F 极附近显红色。
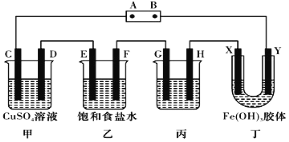
试回答下列问题:
(1)电源 A 极的名称是 ________。
(2)当电路中通过 4 mole-时,要使甲中溶液种类和浓度均复原,可向电解后溶液中加入__________(填某一种物质的化学式和物质的量)。
(3)乙装置中电解反应的总化学方程式为 __________________ 。
(4)若要在丙装置中实现铁器上镀银,银在 _____(填 G 或 H)级。
(5)装置丁中的现象是 _________________________。
(6)若电源用碱性氢氧燃料电池代替,则该电池正极的电极反应式为 ______________ 。
【答案】正极 1molCu(OH)2  G X极附近红褐色变浅,Y极附近红褐色变深 O2+4e-+2H2O=4OH-
G X极附近红褐色变浅,Y极附近红褐色变深 O2+4e-+2H2O=4OH-
【解析】
乙中为饱和食盐水,滴入酚酞溶液,在 F 极附近显红色,说明F电极发生反应2H2O+2e-=H2↑+2OH-,所以F应为阴极,得电子发生还原反应,则B为电源的负极,A为电源的正极。
(1)根据分析可知电源A极为正极;
(2)甲装置中C与电源正极相连为阳极,水电离出的氢氧根放电生成氧气,电极方程式为4OH--4e-=O2↑+2H2O,转移4mol电子时可以产生1molO2;D为阴极,先是铜离子放电生成铜单质,电极方程式为Cu2++2e-=Cu,溶液中n(Cu2+)=1mol,所以转移2mol电子后,铜离子已经完全反应,之后水电离出的氢离子放电产生氢气,电极方程式为2H++2e-=H2↑,又转移2mol电子,所以产生1molH2,则共析出1molO2、1molCu、1molH2,相当于1molCu(OH)2,根据“析出什么补充什么”原则加入物质恢复,需要加入1molCu(OH)2;
(3)乙装置中阳极氯离子放电产生氯气,阴极水电离出的氢离子放电产生氢气,同时产生氢氧根,总反应为 ;
;
(4)因为要在铁器上镀银,所以铁器在阴极,银离子要在阴极发生还原反应生成银单质;同时为了补充电解质溶液中的银离子,需要银单质在阳极发生氧化反应生成银离子,电源的A极为正极,G与A相连,所以银在G极;
(5)根据异性电荷相吸的原理,氢氧化铁胶体中含有的带正电荷的胶体粒子会向阴极Y电极移动,所以X极附近红褐色变浅,Y极附近红褐色变深;
(6)原电池正极得电子发生还原反应,电解质溶液显碱性,所以电极方程式O2+4e-+2H2O=4OH-。

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案【题目】过碳酸钠(2Na2CO33H2O2)俗称固体双氧水。实验室可用碳酸钠和双氧水等为原料来制备,具体流程如下:

已知:①相关反应的方程式如下:2Na2CO3+3H2O2=2Na2CO33H2O2△H<0
②工业上常以产品活性氧的质量分数[ω(活性氧)=![]() ×100%]来衡量产品的优劣,13.00%以上为优等品。
×100%]来衡量产品的优劣,13.00%以上为优等品。
请回答:
表1 反应温度对产品收率及活性氧含量的影响
反应温度/℃ | 产品收率/% | 活性氧质量分数/% |
5 | 65.3 | 12.71 |
10 | 73.2 | 13.24 |
15 | 85.0 | 13.55 |
20 | 83.2 | 13.30 |
25 | 55.1 | 12.78 |
表2加料时间对产品收率及活性氧含量的影响
加料时间/min | 产品收率/% | 活性氧质量分数/% |
5 | 65.7 | 13.30 |
10 | 76.8 | 14.75 |
15 | 81.3 | 14.26 |
20 | 89.0 | 13.82 |
25 | 87.9 | 13.51 |
(1)分析表1,一般选择的反应温度为_____。
(2)分析表2,加料时间对产品收率也有很大影响,时间太短或太长均不利于生产,加料时间太短导致产品收率较低的原因是_____。
(3)结晶过程中加入氯化钠,作用是_____。
(4)下列关于抽滤操作,正确的是_____。
A.准备略大于漏斗内径的滤纸,以盖住布氏漏斗瓷板上的小孔
B.用倾析法先转移溶液,待溶液快流尽时再转移沉淀
C.洗涤沉淀时,加入少量水并开大水龙头,重复操作2~3次
D.用玻璃棒轻轻刮下抽滤得到的固体,晾干后保存在试剂瓶中
(5)使用图2所示装置抽滤,中途需停止抽滤时,最佳操作为_____。
(6)产品出厂前需测定活性氧的质量分数,现将0.1000g某厂的产品(所含杂质均不参与反应)溶于水配成溶液,加入10.00mL1.000molL﹣1的稀硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量_____,用0.1000molL﹣1的Na2S2O3标准溶液滴定,若该产品的活性氧质量分数为13.60%,则达到滴定终点时共消耗标准液的体积为_____mL。[已知:2Na2S2O3+I2=Na2S4O6+2NaI]