题目内容
下列有关微粒性质的排列顺序中,错误的是( )
| A、元素的电负性:P<O<F | B、元素的第一电离能:C<N<O | C、离子半径:O2->Na+>Mg2+ | D、原子的未成对电子数:Mn>Si>Cl |
分析:A、得电子能力越强,电负性越大;
B、元素的第一电离能和最外层电子数的多少有关,轨道处于全充满和半充满状态稳定;
C、电子层越多,半径越大,电子层一样多的微粒,核电荷数越多半径越小;
D、根据原子轨道上电子的排布来确定未成对电子数.
B、元素的第一电离能和最外层电子数的多少有关,轨道处于全充满和半充满状态稳定;
C、电子层越多,半径越大,电子层一样多的微粒,核电荷数越多半径越小;
D、根据原子轨道上电子的排布来确定未成对电子数.
解答:解:A、得电子能力P<O<F,所以元素的电负性P<O<F,故A正确;
B、C的电子排布式:1s22s22p2,N的电子排布式:1s22s22p3,p轨道处于半充满状态,O的电子排布式:1s22s22p4,第一电离能应该是N的最大,故B错误;
C、这些离子是电子层一样多的微粒,根据核电荷数越多半径越小,则离子半径:O2->Na+>Mg2+,故C正确;
D、Mn、Si、Cl原子的未成对电子数分别为5、2、1,即原子的未成对电子数:Mn>Si>Cl,故D正确.
故选B.
B、C的电子排布式:1s22s22p2,N的电子排布式:1s22s22p3,p轨道处于半充满状态,O的电子排布式:1s22s22p4,第一电离能应该是N的最大,故B错误;
C、这些离子是电子层一样多的微粒,根据核电荷数越多半径越小,则离子半径:O2->Na+>Mg2+,故C正确;
D、Mn、Si、Cl原子的未成对电子数分别为5、2、1,即原子的未成对电子数:Mn>Si>Cl,故D正确.
故选B.
点评:本题考查元素及其对应离子、单质、化合物的性质的递变规律,题目难度不大,注意元素的金属性、非金属性与元素性质的递变规律,侧重原子结构及性质的考查.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
 《物质结构与性质》
《物质结构与性质》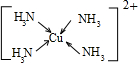

 离子与Ar原子的电子层结构相同。请回答:
离子与Ar原子的电子层结构相同。请回答: 。的稳定结构
。的稳定结构 键 h.
键 h. 键
键
 ,冷水的烧杯中,用玻璃棒不断搅拌,促使晶体析出。用该烧杯中的少量冷水将a内残留的产物冲洗到烧杯中,抽滤,用少量冷水洗涤,得到粗产品。
,冷水的烧杯中,用玻璃棒不断搅拌,促使晶体析出。用该烧杯中的少量冷水将a内残留的产物冲洗到烧杯中,抽滤,用少量冷水洗涤,得到粗产品。