题目内容
【题目】丙烯是仅次于乙烯的有机化工原料,可由丙烷脱氢氧化制取。丙烷脱氢氧化工艺包含的反应有:
主反应:①C3H8(g)![]() C3H6(g)+H2(g) △H1=+124.27 kJ·mol-1(脱氢反应)
C3H6(g)+H2(g) △H1=+124.27 kJ·mol-1(脱氢反应)
②H2(g)+![]() O2(g)=H2O(g) △H2=-241.82 kJ·mol-1(烧氢反应)
O2(g)=H2O(g) △H2=-241.82 kJ·mol-1(烧氢反应)
副反应:③C3H8(g)![]() CH4(g)+C2H4(g) △H3=+81.30 kJ·mol-1
CH4(g)+C2H4(g) △H3=+81.30 kJ·mol-1
④C2H4(g)+H2(g)![]() C2H6(g) △H4=-136.94 kJ·mol-1
C2H6(g) △H4=-136.94 kJ·mol-1
⑤C3H8(g)+H2(g)![]() CH4(g)+C2H6(g) △H5
CH4(g)+C2H6(g) △H5
回答下列问题:
(1)△H5=____kJ·mol-1。
(2)图1是制备工艺中一些反应平衡常数的对数值与温度的关系图,欲提高丙烯的产率,能否尽可能的提高反应温度?_________,其原因是__________________。除温度外,下列还可提高丙烯产率的措施有_________(填序号)

A 降低压强 B 增大压强
C 采用选择性优良的催化剂 D 选择性的氧化消除部分氢气
(3)实际脱氢工艺中常常通入水蒸汽,以改变丙烷的平衡转化率。图2为常压、600~1000K时,不同水烃比M下丙烷脱氢反应的平衡转化率变化图。由图可知,常压、温度恒定时水烃比对平衡转化率的影响规律为____________。设某温度、1 atm(记为p0)下丙烷的脱氢转化率为y,加入反应体系的水蒸汽与原料丙烷的物质的量之比为M,则脱氢反应的平衡常数Kp=____(Kp为以分压表示的平衡常数,写出表达式即可)。
(4)当反应温度为923K时,计算可知脱氢反应的反应热为+115.66 kJ·mol-1,烧氢反应的反应热为-237.75 kJ·mol-1,为保证烧氢所放热量完全满足脱氢吸热之用(假设脱氢率为100%),则烧氢率应大于_____;由此可见,烧氢过程不仅可以提高丙烷脱氢的转化率,还可以_________。
【答案】-55.64 不能 在高温下副反应③比脱氢反应更容易进行 ACD 水烃比越大,脱氢反应平衡转化率越高 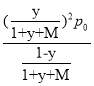 48.6% 降低能耗
48.6% 降低能耗
【解析】
(1)由题目中给出的热化学方程式之间的关系可得![]() =
=![]() +
+![]() ;
;
(2)由图1可知,在高温下副反应③比脱氢反应更容易进行;提高丙烯产率可以使主反应正向进行,或加快主反应速率,抑制副反应的发生;
(3)水烃比值越大,相当于只有烃分解,扩大体积,减小压强,比值越大,正向移动程度越大;根据“三段式”计算出C3H8(g)C3H6(g)+H2(g)平衡时每种物质的物质的量关系,进而进行计算;
(4)烧氢放出的热量为脱氢提供热量,依据量的关系进行计算。
(1)由③C3H8(g)![]() CH4(g)+C2H4(g) △H3=+81.30 kJ·mol-1
CH4(g)+C2H4(g) △H3=+81.30 kJ·mol-1
④C2H4(g)+H2(g)![]() C2H6(g) △H4=-136.94 kJ·mol-1
C2H6(g) △H4=-136.94 kJ·mol-1
可知⑤C3H8(g)+H2(g)![]() CH4(g)+C2H6(g)可以由③+④得到,所以
CH4(g)+C2H6(g)可以由③+④得到,所以![]() =
=![]() +
+![]() =+81.30kJ·mol-1+(-136.94kJ·mol-1)=-55.64kJ·mol-1;
=+81.30kJ·mol-1+(-136.94kJ·mol-1)=-55.64kJ·mol-1;
(2)由图可知,欲提高丙烯的产率,不能尽可能的提高反应温度,因为在高温下副反应③比脱氢反应更容易进行;降低压强、选择性的氧化消除部分氢气可以使主反应正向进行,采用选择性优良的催化剂可以加快主反应速率,降低副反应进行程度,提高丙烯产率;
(3)水烃比值越大,相当于只有烃分解,扩大体积,减小压强;比值越大,正向移动程度越大,即水烃比越大,脱氢反应平衡转化率越高;
假设丙烷为1mol,则有:
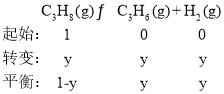
Kp=![]() =
= =
=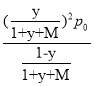 ;
;
(4)由题意可知,烧氢放出的热量为脱氢提供热量,依据量的关系可得:烧氢率应大于![]() =48.6%,由此可见,烧氢过程不仅可以提高丙烷脱氢的转化率,还可以降低能耗。
=48.6%,由此可见,烧氢过程不仅可以提高丙烷脱氢的转化率,还可以降低能耗。

 名校课堂系列答案
名校课堂系列答案