题目内容
【题目】过氧化钙,化学式为CaO2,微溶于水,溶于酸,可用作分析试剂、医用防腐剂、消毒剂。现有一种制备过氧化钙的实验方案,流程如下图,其主要反应的化学方程式为:CaCl2+2NH3·H2O+H2O2=CaO2↓+2NH4Cl+2H2O表示。回答下列问题:
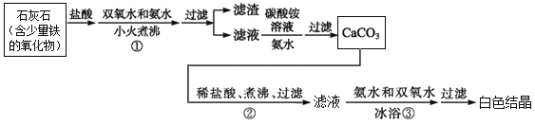
(1)步骤①中,加入氨水的目的是_____________,小火煮沸的作用是________________________。
(2)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体;再将溶液煮沸,趁热过滤。此过程中,将溶液煮沸的作用是________________________________________。
(3)制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到产品。此法工艺简单、操作方便,但是得到的产品纯度较低,往往CaCO3、Ca(OH)2等杂质含量较高。若实验室只提供稀盐酸和澄清石灰水两瓶试剂,以及试管、小烧杯、胶头滴管、药匙各1个,请设计实验检验所得产品中含有CaCO3。_____________________________(简要描述方案即可)。
【答案】调节溶液pH使Fe(OH)3沉淀使沉淀颗粒长大,有利于过滤分离使Ca(HCO3)2分解,并驱除溶解的CO2取少量产品于试管中,加入稀盐酸,立即在试管口上方倒扣内涂澄清石灰水的小烧杯;若产生白色沉淀,则产品中含CaCO3。
【解析】
由流程可知,加盐酸,碳酸钙、铁的氧化物均溶解,加双氧水可氧化亚铁离子,加氨水将铁离子转化为沉淀,过滤后的滤液中含盐酸,加氨水中和酸,利用得到碳酸钙沉淀;碳酸钙溶于盐酸后,至溶液中尚存有少量固体,过滤后,滤液中氯化钙、氨水、过氧化氢在冰水浴中反应生成CaO2、NH4Cl、水;再过滤,洗涤得到过氧化钙。
(1)步骤①加入氨水的目的是中和多余的盐酸,沉淀铁离子;小火煮沸的作用是使沉淀颗粒长大,有利于过滤,故答案为:调节溶液pH使Fe(OH)3沉淀;使沉淀颗粒长大,有利于过滤分离;
(2)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,溶液中溶解二氧化碳,此时溶液呈酸性;将溶液煮沸,趁热过滤,将溶液煮沸的作用是使Ca(HCO3)2分解,并除去溶液中溶解的二氧化碳,故答案为:使Ca(HCO3)2分解,并除去溶液中溶解的二氧化碳;
(3)碳酸钙与盐酸反应生成二氧化碳,只要检验是否生成了二氧化碳即可,实验方案为:取少量产品于试管中,加入稀盐酸,立即在试管口上方倒扣内涂澄清石灰水的小烧杯;若产生白色沉淀,则产品中含CaCO3,故答案为:取少量产品于试管中,加入稀盐酸,立即在试管口上方倒扣内涂澄清石灰水的小烧杯;若产生白色沉淀,则产品中含CaCO3。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案