题目内容
【题目】由多元素组成的化合物Fe-Sm-As-F-O是一种重要的铁系超导材料。下列说法正确的是
A.F的核外电子排布式1s22s22p7
B.Fe3+的轨道表示式![]() 违背了泡利不相容原理
违背了泡利不相容原理
C.N、As同主族,第一电离能N<As
D.电负性F>O>As
【答案】D
【解析】
A.氟原子核外电子数为9,基态氟原子核外电子排布式为1s22s22p5,故A错误;
B.泡利不相容原理内容为:每个原子轨道上最多只能容纳2个自旋状态相反的电子,选项中违背洪特规则,铁离子3d轨道排布图应为: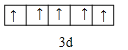 ,故B错误;
,故B错误;
C.N、As同主族,同一主族元素第一电离能随着原子序数增大而减小,所以第一电离能N>As,故C错误;
D.同一周期元素从左到右电负性逐渐增大,电负性F>O>N,同一主族元素从上到下电负性逐渐减小,电负性N>As,所以电负性F>O>As,故D正确;
故选:D。

练习册系列答案
相关题目
【题目】实验室用少量的溴和足量的乙醇制备1,2一二溴乙烷的装置如图所示:
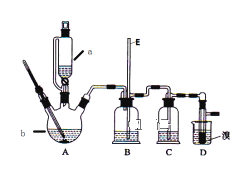
有关数据列表如下:
乙醇 | 1.2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g/cm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣130 | 9 | ﹣116 |
请按要求回答下列问题:
(1)写出A装置中的化学反应方程式_____;
(2)装置C中盛有氢氧化钠溶液,其作用是_____
(3)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_____
(4)判断该制备反应已经结束的最简单方法是_____;
(5)若产物中有少量未反应的Br2,最好用_____洗涤除去;(填正确选项前的字母)
a 水 b 亚硫酸氢钠 c 碘化钠溶液 d 乙醇
(6)反应过程中应用冷水冷却装置D,其主要目的是_____;但又不能过度冷却(如用冰水),其原因是_____.