题目内容
【题目】为探究碳酸氢钠的热稳定性,并利用其产物验证过氧化钠与二氧化碳的反应,按以下装置图进行实验,按要求填空。
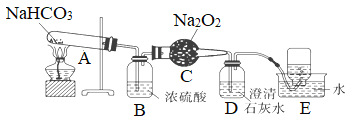
(1)A中反应的化学方程式为________________________________。
(2)B中浓硫酸的作用是__________________。
(3)C中发生反应的化学方程式为_________________________________。
(4)D中反应的离子方程式是_______________________________。
(5)E中收集的气体主要是________。
【答案】2NaHCO3![]() Na2CO3+CO2↑+H2O 干燥二氧化碳 2Na2O2+2CO2=2Na2CO3+O2 Ca2++2OH+CO2=CaCO3↓+H2O O2
Na2CO3+CO2↑+H2O 干燥二氧化碳 2Na2O2+2CO2=2Na2CO3+O2 Ca2++2OH+CO2=CaCO3↓+H2O O2
【解析】
探究碳酸氢钠的热稳定性,并利用其产物验证过氧化钠与二氧化碳的反应,由实验装置可知,A中碳酸氢钠分解生成二氧化碳,B中浓硫酸干燥气体,C中发生2Na2O2+2CO2=2Na2CO3+O2,D中吸收二氧化碳,E为排水法收集氧气,以此来解答。
(1)A中反应为碳酸氢钠受热分解的反应,化学方程式为2NaHCO3![]() Na2CO3+CO2↑+H2O,
Na2CO3+CO2↑+H2O,
故答案为:2NaHCO3![]() Na2CO3+CO2↑+H2O ;
Na2CO3+CO2↑+H2O ;
(2)B中浓硫酸的作用是干燥二氧化碳,故答案为:干燥二氧化碳;
(3)C中发生反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(4)D中吸收二氧化碳,离子方程式为Ca2++2OH-+CO2=CaCO3↓+H2O,故答案为: Ca2++2OH-+CO2=CaCO3↓+H2O;
(5)E中收集的气体主要是O2,故答案为:O2。

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目