题目内容
【题目】在容积一定的密闭容器中,可逆反应A(g)+B(g)xC(g),有如图所示的关系曲线,根据下图下列判断正确的是( ) 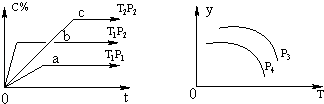
A.p3>p4 , y轴表示A的转化率
B.p3<p4 , y轴表示混合气体的密度
C.p3<p4 , y轴表示B的质量分数
D.p3<p4 , y轴表示混合气体的平均摩尔质量
【答案】A
【解析】解:依据图(Ⅰ)中a、b的相对位置知,增压(因p2>p1),w(C)升高,故x=1;由b、c的相对位置知,升温(因为T1>T2),w(C)降低,故正反应为放热反应.
即该反应为:A(g)+B(g) ![]() C(g)(正反应为放热反应),由反应式可知,升温和降压均可使反应向逆反应方向移动.
C(g)(正反应为放热反应),由反应式可知,升温和降压均可使反应向逆反应方向移动.
由图(Ⅱ)知:因升温y降低,故y降低的方向必为压强减小的方向,所以,P3>P4 , 随着温度的升高,平衡将向左移动,A的转化率降低;随着压强的减小,A物质的转化率减小,
只有A符合P3>P4 ,
故选A.

 优等生题库系列答案
优等生题库系列答案【题目】用NH3催化还原NxOy可以消除氮氧化物的污染.已知:反应I:4NH3(g)+6NO(g)5N2(g)+6H2O(l)△H1
反应II:2NO(g)+O2(g)2NO2(g)△H2 (且|△H1|=2|△H2|)
反应III:4NH3(g)+6NO2(g)5N2(g)+3O2(g)+6H2O(l)△H3
反应I和反应II在不同温度时的平衡常数及其大小关系如下表
温度/K | 反应I | 反应II | 已知: |
298 | K1 | K2 | |
398 | K1′ | K2′ |
(1)推测反应III是反应(填“吸热”或“放热”)
(2)相同条件下,反应I在2L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图1所示.①计算0~4分钟在A催化剂作用下,反应速率v(NO)= .
②下列说法正确的是 .
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
B.增大压强能使反应速率加快,是因为增加了活化分子百分数
C.单位时间内H﹣O键与N﹣H键断裂的数目相等时,说明反应已经达到平衡
D.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
(3)一定条件下,反应II达到平衡时体系中n(NO):n(O2):n(NO2)=2:1:2.在其它条件不变时,再充入NO2气体,分析NO2体积分数﹣﹣φ(NO2)的变化情况:(填“变大”、“变小”或“不变”)恒温恒压容器,φ(NO2);恒温恒容容器,φ(NO2) .
(4)一定温度下,反应III在容积可变的密闭容器中达到平衡,此时容积为3L,c(N2)与反应时间t变化曲线X如图2所示,若在t1时刻改变一个条件,曲线X变为曲线Y或曲线Z.则:①变为曲线Y改变的条件是 . 变为曲线Z改变的条件是 . 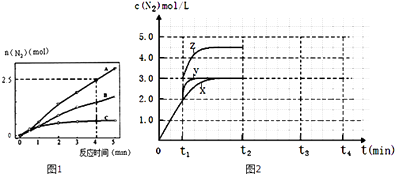
②若t2降低温度,t3达到平衡,请在上图中画出曲线X在t2﹣t4内 c(N2)的变化曲线 .