题目内容
20.标准状况下,1mol H2和1mol H2O相同的是( )| A. | 质量 | B. | 体积 | C. | 原子数 | D. | 分子数 |
分析 结合m=nM、V=nVm、N=nNA及分子构成计算.
解答 解:A.M分别为2g/mol、18g/mol,则等物质的量时质量不同,故A错误;
B.由V=nVm可知,物质的量相同,Vm相同,则体积相同,故B正确;
C.1mol H2和1mol H2O,含原子分别为2mol、3mol,则原子数不同,故C错误;
D.由N=nNA可知,物质的量相同,则分子数相同,故D正确‘
故选BD.
点评 本题考查物质的量的计算,为高频考点,把握物质的量、质量、体积的关系为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
10.右下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍.下列说法不正确的是( )
| X | ||
| Y | Z | W |
| T |
| A. | X、W、Z元素的气态氢化物的热稳定性依次递减 | |
| B. | 液态WX3气化需克服分子间作用力 | |
| C. | 根据元素周期律,可以推测T元素的单质具有半导体特性 | |
| D. | Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 |
11.在热的稀硫酸溶液中溶解了45.6gFeSO4.当加入200mL0.5mol•L-1KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3溶液也完全反应,并有NxOy气体逸出,则该NxOy是( )
| A. | N2O | B. | NO | C. | N2O3 | D. | NO2 |
5.下列每组中的两对物质,都能用分液漏斗分离且油层由分液漏斗上口倒出的是( )
| A. | 汽油和水,四氯化碳和水 | B. | 汽油和水,苯和水 | ||
| C. | 食用油和水,醋酸和水 | D. | 葡萄糖和水,酒精和水 |
12.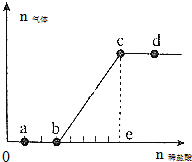 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.下列有关说法中正确的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.下列有关说法中正确的是( )
 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.下列有关说法中正确的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.下列有关说法中正确的是( )| A. | a点对应的溶液中c(CO${\;}_{3}^{2-}$)>c(HCO${\;}_{3}^{-}$) | |
| B. | b,c段反应的离子方程式为HCO${\;}_{3}^{-}$+H+═H2O+CO2↑ | |
| C. | 原溶液中n(NaCO3)=n(NaHCO3) | |
| D. | K+、NO${\;}_{3}^{-}$、SiO${\;}_{3}^{2-}$可大量存在于d点对应的溶液中 |
9.在0.1L某浓度的NaCl溶液中含有0.8mol Na+,下列对该溶液的说法中,不正确的是( )
| A. | 量取10mL该溶液倒入试管中,试管中,试管中Na+的物质的量为0.08mol | |
| B. | 该溶液的物质的量浓度为0.8mol•L-1 | |
| C. | 该溶液中含有46.8g NaCl | |
| D. | 配置50mL该溶液需用23.4g NaCl |
19.根据表中信息判断.下列选项正确的是( )
| 序号 | 反应物(均反应完全) | 生成物 |
| ① | Cl2、H2O2 | O2、… |
| ② | KMnO4,H2O2,H2SO4 | K2SO4、MnSO4… |
| ③ | Cl2、FeBr2 | FeCl3.FeBr3 |
| A. | ①反应中生成1molO2,转移4mole- | |
| B. | ②反应中的其余生成物只有H2O | |
| C. | ③反应中n(Cl2):n(FeBr2)=n(FeCl3):n(FeBr3)=1:2 | |
| D. | 由表知氧化性由强到弱顺序:MnO${\;}_{4}^{-}$>Cl2>H2O2>Fe2+>Br2 |