题目内容
9.有机物M是一种重要的化工原料,已知M分子式为C7H14O2,1mol M最多消耗46g金属钠.M可通过下列路线合成(某些反应的反应物和反应条件未列出):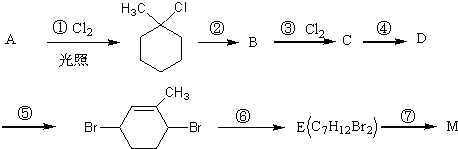
(1)按要求写出结构简式:A
 C
C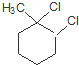 M
M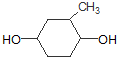
(2)写出反应①、④、的化学方程式:①
 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl④
+HCl④ +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$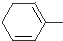 +2NaOH+2H2O
+2NaOH+2H2O(3)⑥的反应类型是加成(或还原)反应.
(4)写出M中所含官能团的名称羟基.
分析 M分子式为C7H14O2,1mol M最多消耗46g金属钠,则可知M中有两个醇羟基,根据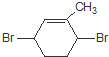 可知M中有六元环,反应⑥为
可知M中有六元环,反应⑥为 与氢气的加成得E,反应⑦为碱性水解,将E中的两个溴原子取代成羟基,所以可推得M为
与氢气的加成得E,反应⑦为碱性水解,将E中的两个溴原子取代成羟基,所以可推得M为 ,据M的结构可反应推E为
,据M的结构可反应推E为 ,根据
,根据 可反推得A为
可反推得A为 ,
, 发生消去反应生成B为
发生消去反应生成B为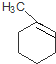 ,
, 与氯气加成得C为
与氯气加成得C为 ,
, 发生消去反应得D为
发生消去反应得D为 ,据此答题.
,据此答题.
解答 解:M分子式为C7H14O2,1mol M最多消耗46g金属钠,则可知M中有两个醇羟基,根据 可知M中有六元环,反应⑥为
可知M中有六元环,反应⑥为 与氢气的加成得E,反应⑦为碱性水解,将E中的两个溴原子取代成羟基,所以可推得M为
与氢气的加成得E,反应⑦为碱性水解,将E中的两个溴原子取代成羟基,所以可推得M为 ,据M的结构可反应推E为
,据M的结构可反应推E为 ,根据
,根据 可反推得A为
可反推得A为 ,
, 发生消去反应生成B为
发生消去反应生成B为 ,
, 与氯气加成得C为
与氯气加成得C为 ,
, 发生消去反应得D为
发生消去反应得D为 ,
,
(1)根据上面的分析可知,A为 ,C为
,C为 ,M为
,M为 ,
,
故答案为: ;
; ;
; ;
;
(2)反应①方程式为 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl,反应④的方程式为
+HCl,反应④的方程式为 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaOH+2H2O,
+2NaOH+2H2O,
故答案为: +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl;
+HCl; +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaOH+2H2O;
+2NaOH+2H2O;
(3)根据上面的分析可知,⑥的反应类型是加成(或还原)反应,
故答案为:加成(或还原)反应;
(4)M为 ,M中所含官能团的名称是羟基,
,M中所含官能团的名称是羟基,
故答案为:羟基.
点评 本题考查有机物物的合成与推断,题目难度不大,注意把握有机物官能团的变化以及反应条件,本题可用正推和逆推相结合的方法进行推断.

练习册系列答案
相关题目
20.下列关于燃料的说法错误的是( )
| A. | 煤可以气化得到发生炉煤气、水煤气、焦炉气,这些气体都含有CO | |
| B. | 液化石油气的成分不同于天然气,容易冒黑烟 | |
| C. | 沼气因使用具有危险性,不能推广使用 | |
| D. | 燃料电池能源的利用率高、污染少,具有很好的应用前景 |
17.下列关于二氧化硅的说法中,不正确的是( )
| A. | 能与水反应 | B. | 能与NaOH溶液反应 | ||
| C. | 能与氢氟酸反应 | D. | 能与氧化钙反应 |
4.有关水的电离平衡的说法正确的是( )
| A. | 水的离子积Kw、随温度变化而变化,在稀盐酸中数值会变大 | |
| B. | 在纯水中加入硫酸会抑制水的电离,加醋酸会促进水的电离 | |
| C. | 向水中加入NaHSO4溶液,抑制水的电离,溶液呈酸性 | |
| D. | 向水中加入NH4Cl溶液,促进水的电离,溶液呈碱性 |
14.下列四个能级中,能量最高,电子最后填充的是( )
| A. | 3s | B. | 3p | C. | 3d | D. | 4s |
1. 科学家根据自然界存在的N2制取出N3,又陆续制取出N5+、N4H44+等离子.已知N4H44+的空间构型如图,下列说法正确的是( )
科学家根据自然界存在的N2制取出N3,又陆续制取出N5+、N4H44+等离子.已知N4H44+的空间构型如图,下列说法正确的是( )
 科学家根据自然界存在的N2制取出N3,又陆续制取出N5+、N4H44+等离子.已知N4H44+的空间构型如图,下列说法正确的是( )
科学家根据自然界存在的N2制取出N3,又陆续制取出N5+、N4H44+等离子.已知N4H44+的空间构型如图,下列说法正确的是( )| A. | N3和N2互为同位素 | |
| B. | 7.0gN5+离子含有34×6.02×1022个电子 | |
| C. | N5+中氮、氮原子间形成离子键 | |
| D. | N4H44+的4个H共平面 |
19.已知:常温时;2NaOH+Cl2═NaCl+NaClO+H2O;加热时:6NaOH+3Cl2═5NaCl+NaClO3+3H2O,将Cl2通入amol NaOH溶液恰好完全反应,下列有关说法错误的是( )
| A. | 参加反应的氯气的物质的量等于0.5a mo1 | |
| B. | 若某温度下,反应后$\frac{c(Cl{O}^{-})}{c(Cl{O}_{3}^{-}})$=K,若溶液中$\frac{c(Cl{O}^{-})}{c(C{l}^{-})}$=$\frac{K}{K+5}$ | |
| C. | 控制温度,反应中转移电子的物质的量最大值是a mol | |
| D. | 控制温度,产物中NaCl的物质的量的范围$\frac{1}{2}$a mol≤n(NaCl)≤$\frac{5}{6}$a mol |

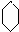 ;名称是环己烷.
;名称是环己烷.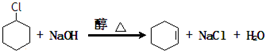 .
.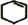 +Br2→
+Br2→ .
.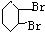 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$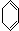 +2NaBr+2H2O.
+2NaBr+2H2O.