题目内容
1. 科学家根据自然界存在的N2制取出N3,又陆续制取出N5+、N4H44+等离子.已知N4H44+的空间构型如图,下列说法正确的是( )
科学家根据自然界存在的N2制取出N3,又陆续制取出N5+、N4H44+等离子.已知N4H44+的空间构型如图,下列说法正确的是( )| A. | N3和N2互为同位素 | |
| B. | 7.0gN5+离子含有34×6.02×1022个电子 | |
| C. | N5+中氮、氮原子间形成离子键 | |
| D. | N4H44+的4个H共平面 |
分析 A.同位素是指质子数相同中子数不同的同种元素的不同原子;
B.1个N5+含有34个电子,先求出离子的物质的量,再求出电子的物质的量和数目;
C.非金属原子间形成共价键;
D.根据N4H44+的结构图分析.
解答 解:A.同位素的研究对象为原子,N4与N2都是单质,故A错误;
B.1个N5+含有34个电子,7.0gN5+离子的物质的量为0.1mol,则电子的物质的量为3.4mol,即含有34×6.02×1022个电子,故B正确;
C.非金属原子间形成共价键,则N5+中氮、氮原子间形成共价键,故C错误;
D.由题干中N4H44+的结构图可知,为正四面体结构,所以只有3个H原子共面,故D错误;
故选:B.
点评 本题为信息题,考查了同位素的概念和化学键类型的判断,电子数的计算方法,解题时要充分利用题给信息,结合有关概念分析判断,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 标准状况下,1L乙烷所含有的分子数为NA/22.4 | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 常温下,28g C2H4含NA个碳碳双键 | |
| D. | 1L0.1mol•L-1乙酸溶液中H+数为0.1NA |
12.下列对一些实验事实的理论解释不正确的是( )
| 选项 | 实验事实 | 理论解释 |
| A | 酸性:H3BO3、H2SiO3均为弱酸 | B、Si电负性相近,符合“对角线规则” |
| B | 熔点:SiO2>SiCl4 | 键能:Si-O>Si-Cl |
| C | 密度:干冰>冰 | 干冰晶体为分子密堆积 |
| D | 沸点:NO>O2>N2 | NO为极性分子;且相对分子质量:O2>N2 |
| A. | A | B. | B | C. | C | D. | D |
16.下列说法正确的是( )
| A. | 在元素周期表中,s区、d区和ds区的元素都是金属 | |
| B. | 可能存在核外电子排布为1s22s22p63s23p64s24p1的原子 | |
| C. | 能层序数越大,s原子轨道的半径越大 | |
| D. | 在同一能级上运动的电子,其运动状态一定相同 |
10.元素原子最外层电子层上只有一个电子,该元素( )
| A. | 一定是金属元素 | B. | 不一定是金属元素 | ||
| C. | 一定是ⅠA族元素 | D. | 一定是非主族元素 |
11.下列关于硫酸铜溶液的说法中,不正确的是( )
| A. | 硫酸铜水解使溶液呈酸性 | |
| B. | 升温可促进硫酸铜的水解 | |
| C. | 滴入几滴浓硫酸,硫酸铜的水解程度减小 | |
| D. | 加入少量的硫酸氢钠固体,不影响硫酸铜的水解 |
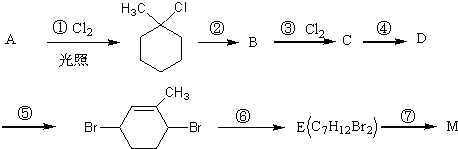
 C
C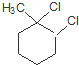 M
M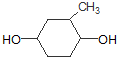
 +HCl④
+HCl④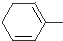 +2NaOH+2H2O
+2NaOH+2H2O