题目内容
已知某饱和NaCl溶液的体积为V mL,密度为ρ g/cm3,质量分数为w%,物质的量浓度为c mol/L,溶液中含NaCl的质量为m g。
(1)用m、V表示溶液的物质的量浓度_____________________。
(2)用w、ρ表示溶液物质的量浓度____________________。
(3)用c、ρ表示溶液的质量分数__________________。
(4)用w表示该温度下NaCl的溶解度____________________。
(1)用m、V表示溶液的物质的量浓度_____________________。
(2)用w、ρ表示溶液物质的量浓度____________________。
(3)用c、ρ表示溶液的质量分数__________________。
(4)用w表示该温度下NaCl的溶解度____________________。
(1)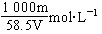
(2)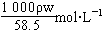
(3)
(4)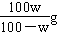
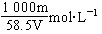
(2)
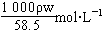
(3)

(4)
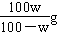

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
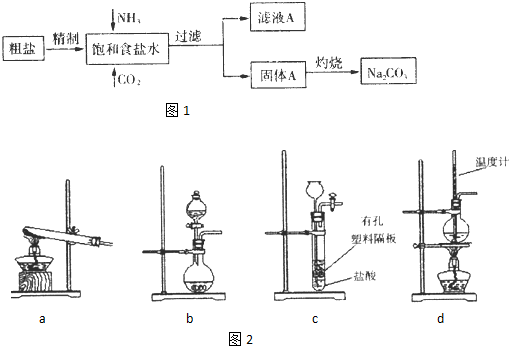
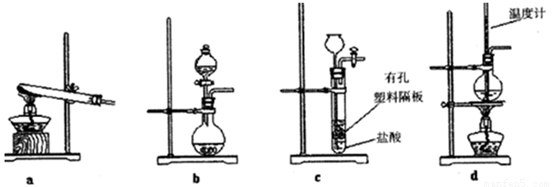
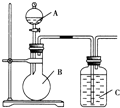 某同学设计如图装置,研究非金属元素性质变化规律.
某同学设计如图装置,研究非金属元素性质变化规律.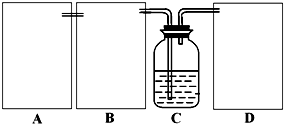
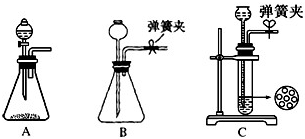
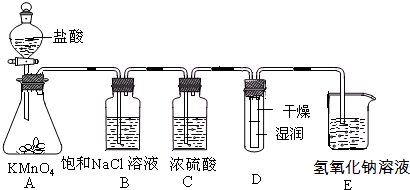
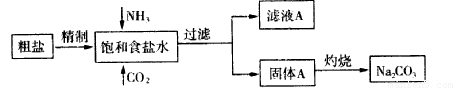
 NaHCO3↓+NH4Cl,请回答以下问题:
NaHCO3↓+NH4Cl,请回答以下问题: