��Ŀ����
��2011?��̨��һģ����ҵ�Ͻ��������������ͨ�뵽���ʵ���Ũ��Ϊ0.375mol/LNaOH��Һ�еõ�Ưˮ��ijͬѧ����ʵ����̽��Cl2���ʲ�ģ���Ʊ�Ưˮ����ͼ�Dz���ʵ��װ�ã���֪KMnO4��������Һ��Ӧ������ȡCl2��
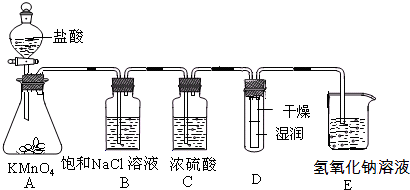
��1���������ʵ���Ũ��Ϊ0.375mol/LNaOH��Һʱ����Ҫ�õ��IJ����������ձ�������������ͷ�ιܡ���Ͳ��
��2��Ũ�����������
��3��װ��E�з�����ѧ��Ӧ�����ӷ���ʽΪ
��4��װ��B�б���NaCl��Һ�����ڳ�ȥCl2�е�HCl���壬��֪������ˮ�ķ�Ӧ��һ�����淴Ӧ�����������NaCl��Һ��ȥCl2��HCl�����ԭ���������ӷ���ʽ��ʾ������˵����
��5��ʵ��ʱװ��D��ʪ��ĺ�ɫֽ����ɫ�����ﲿ��û����ɫ������һ��ʱ���ֽ��ȫ����ɫ����ͬѧ��ΪCl2���ܶȱȿ����������Թ��²�Cl2��Ũ�ȴ����Թ��ϲ�Cl2��Ũ�������µģ����жϸý����Ƿ����
��6����Ԫ�غ���Ϊ10%��Ưˮ��Һ355g�����к�NaClO�����ʵ���Ϊ

��1���������ʵ���Ũ��Ϊ0.375mol/LNaOH��Һʱ����Ҫ�õ��IJ����������ձ�������������ͷ�ιܡ���Ͳ��
����ƿ
����ƿ
����2��Ũ�����������
��������
��������
����3��װ��E�з�����ѧ��Ӧ�����ӷ���ʽΪ
Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
����4��װ��B�б���NaCl��Һ�����ڳ�ȥCl2�е�HCl���壬��֪������ˮ�ķ�Ӧ��һ�����淴Ӧ�����������NaCl��Һ��ȥCl2��HCl�����ԭ���������ӷ���ʽ��ʾ������˵����
HCl����ˮ�������H+�ͱ���NaCl��Һ�е�Cl-����Է�ӦCl2+H2O?H++Cl-+HClO����������
HCl����ˮ�������H+�ͱ���NaCl��Һ�е�Cl-����Է�ӦCl2+H2O?H++Cl-+HClO����������
����5��ʵ��ʱװ��D��ʪ��ĺ�ɫֽ����ɫ�����ﲿ��û����ɫ������һ��ʱ���ֽ��ȫ����ɫ����ͬѧ��ΪCl2���ܶȱȿ����������Թ��²�Cl2��Ũ�ȴ����Թ��ϲ�Cl2��Ũ�������µģ����жϸý����Ƿ����
������
������
����������������ʵ�������ԭ��ʵ�������Cl2��ʪ���ɫֽ���е�ˮ��Ӧ����HClOʹʪ��ĺ�ɫֽ����ɫ�����ﲿ��û��HClO������ֽ������ɫ������һ��ʱ�䣬����ˮ�����˶��ᵼ������ֽ��ʪ�����ɫ
ʵ�������Cl2��ʪ���ɫֽ���е�ˮ��Ӧ����HClOʹʪ��ĺ�ɫֽ����ɫ�����ﲿ��û��HClO������ֽ������ɫ������һ��ʱ�䣬����ˮ�����˶��ᵼ������ֽ��ʪ�����ɫ
������Ľ����������Ʒ���ȡһ���ϰ彫����ĺ�ɫֽ����ʪ��ĺ�ɫֽ���ֱ��������ϰ����࣬����װ�÷���װ��D�л�������ͨ��װ�и���ĺ�ɫֽ�����Թܣ���ͨ��װ��ʪ��ĺ�ɫֽ�����Թ���
ȡһ���ϰ彫����ĺ�ɫֽ����ʪ��ĺ�ɫֽ���ֱ��������ϰ����࣬����װ�÷���װ��D�л�������ͨ��װ�и���ĺ�ɫֽ�����Թܣ���ͨ��װ��ʪ��ĺ�ɫֽ�����Թ���
������Ϊ����������ʿɲ����𣩣���6����Ԫ�غ���Ϊ10%��Ưˮ��Һ355g�����к�NaClO�����ʵ���Ϊ
0.5
0.5
mol����������1��������Һ�������õ���������������
��2��Ũ���������ˮ�ԣ��������������壻
��3�������ж��������ŷ��ڻ����У���NaOH��Һ���գ�
��4���������ӵ�Ũ��������ƽ���ƶ���
��5��������������ʹ��ɫ������ɫ��HClOʹ��ɫ��������ɫ��ˮ���ӵ��˶���������
��6����Ԫ�غ���Ϊ10%��Ưˮ��Һ355g����m��Cl��=35.5g��n��Cl��=1mol��������n��Cl��=n��NaCl��+n��NaClO����Cl2+2NaOH�TNaCl+NaClO+H2O��������
��2��Ũ���������ˮ�ԣ��������������壻
��3�������ж��������ŷ��ڻ����У���NaOH��Һ���գ�
��4���������ӵ�Ũ��������ƽ���ƶ���
��5��������������ʹ��ɫ������ɫ��HClOʹ��ɫ��������ɫ��ˮ���ӵ��˶���������
��6����Ԫ�غ���Ϊ10%��Ưˮ��Һ355g����m��Cl��=35.5g��n��Cl��=1mol��������n��Cl��=n��NaCl��+n��NaClO����Cl2+2NaOH�TNaCl+NaClO+H2O��������
����⣺��1������һ�����ʵ���Ũ�ȵ���Һʹ�õIJ����������ձ�������������ͷ�ιܡ���Ͳ������ƿ��
�ʴ�Ϊ������ƿ��
��2����Ũ���������ˮ�ԣ��Ҳ���������Ӧ����װ��C��Ũ���������Ϊ�����������ʴ�Ϊ������������
��3��δ�μӷ�Ӧ�����������ŷ��ڻ����У���װ��EΪ����β����װ�ã������ӷ�ӦΪCl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
��4����������ˮ����Cl2+H2O?H++Cl-+HClO����HCl����ˮ�������H+�ͱ���NaCl��Һ�е�Cl-����Է�ӦCl2+H2O?H++Cl-+HClO���������ã�������ñ���NaCl��Һ��ȥCl2��HCl���壬
�ʴ�Ϊ��HCl����ˮ�������H+�ͱ���NaCl��Һ�е�Cl-����Է�ӦCl2+H2O?H++Cl-+HClO���������ã�
��5������������ʹ��ɫ������ɫ��HClOʹ��ɫ��������ɫ����һ��ʱ���ˮ�������˶�������ĺ�ɫֽ���У���ʵ�鲻�����������ʵ���ҽ�ʪ��ĺ�ɫֽ��������ֽ�����룬�����Ϊȡһ���ϰ彫����ĺ�ɫֽ����ʪ��ĺ�ɫֽ���ֱ��������ϰ����࣬����װ�÷���װ��D�л�������ͨ��װ�и���ĺ�ɫֽ�����Թܣ���ͨ��װ��ʪ��ĺ�ɫֽ�����Թ��У�
�ʴ�Ϊ����������ʵ�������Cl2��ʪ���ɫֽ���е�ˮ��Ӧ����HClOʹʪ��ĺ�ɫֽ����ɫ�����ﲿ��û��HClO������ֽ������ɫ������һ��ʱ�䣬����ˮ�����˶��ᵼ������ֽ��ʪ�����ɫ��ȡһ���ϰ彫����ĺ�ɫֽ����ʪ��ĺ�ɫֽ���ֱ��������ϰ����࣬����װ�÷���װ��D�л�������ͨ��װ�и���ĺ�ɫֽ�����Թܣ���ͨ��װ��ʪ��ĺ�ɫֽ�����Թ��У�
��6����Ԫ�غ���Ϊ10%��Ưˮ��Һ355g����m��Cl��=��10%=35.5g��n��Cl��=
=1mol��
��Cl2+2NaOH�TNaCl+NaClO+H2O��֪��
n��Cl��=n��NaCl��+n��NaClO������n��NaClO��=
=0.5mol���ʴ�Ϊ��0.5��
�ʴ�Ϊ������ƿ��
��2����Ũ���������ˮ�ԣ��Ҳ���������Ӧ����װ��C��Ũ���������Ϊ�����������ʴ�Ϊ������������
��3��δ�μӷ�Ӧ�����������ŷ��ڻ����У���װ��EΪ����β����װ�ã������ӷ�ӦΪCl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
��4����������ˮ����Cl2+H2O?H++Cl-+HClO����HCl����ˮ�������H+�ͱ���NaCl��Һ�е�Cl-����Է�ӦCl2+H2O?H++Cl-+HClO���������ã�������ñ���NaCl��Һ��ȥCl2��HCl���壬
�ʴ�Ϊ��HCl����ˮ�������H+�ͱ���NaCl��Һ�е�Cl-����Է�ӦCl2+H2O?H++Cl-+HClO���������ã�
��5������������ʹ��ɫ������ɫ��HClOʹ��ɫ��������ɫ����һ��ʱ���ˮ�������˶�������ĺ�ɫֽ���У���ʵ�鲻�����������ʵ���ҽ�ʪ��ĺ�ɫֽ��������ֽ�����룬�����Ϊȡһ���ϰ彫����ĺ�ɫֽ����ʪ��ĺ�ɫֽ���ֱ��������ϰ����࣬����װ�÷���װ��D�л�������ͨ��װ�и���ĺ�ɫֽ�����Թܣ���ͨ��װ��ʪ��ĺ�ɫֽ�����Թ��У�
�ʴ�Ϊ����������ʵ�������Cl2��ʪ���ɫֽ���е�ˮ��Ӧ����HClOʹʪ��ĺ�ɫֽ����ɫ�����ﲿ��û��HClO������ֽ������ɫ������һ��ʱ�䣬����ˮ�����˶��ᵼ������ֽ��ʪ�����ɫ��ȡһ���ϰ彫����ĺ�ɫֽ����ʪ��ĺ�ɫֽ���ֱ��������ϰ����࣬����װ�÷���װ��D�л�������ͨ��װ�и���ĺ�ɫֽ�����Թܣ���ͨ��װ��ʪ��ĺ�ɫֽ�����Թ��У�
��6����Ԫ�غ���Ϊ10%��Ưˮ��Һ355g����m��Cl��=��10%=35.5g��n��Cl��=
| 35.5g |
| 35.5g/mol |
��Cl2+2NaOH�TNaCl+NaClO+H2O��֪��
n��Cl��=n��NaCl��+n��NaClO������n��NaClO��=
| 1mol |
| 2 |
���������⿼����������ȡʵ��װ�ü����������ʣ���ȷװ�õ����ü�װ���з����Ļ�ѧ��Ӧ���ɽ���ѶȲ������÷�Ӧ������������ѧ���ڽ�������ӵĵط���

��ϰ��ϵ�д�
�����Ŀ
 ��2011?��̨��һģ�������£���0.1000mol/L NaOH��Һ�ֱ�ζ�20.00mL 0.1000mol/L �����20.00mL 0.1000mol/L ������Һ���õ�2���ζ����ߣ���ͼ��ʾ������HA��ʾ�ᣬ����˵����ȷ���ǣ�������
��2011?��̨��һģ�������£���0.1000mol/L NaOH��Һ�ֱ�ζ�20.00mL 0.1000mol/L �����20.00mL 0.1000mol/L ������Һ���õ�2���ζ����ߣ���ͼ��ʾ������HA��ʾ�ᣬ����˵����ȷ���ǣ������� ��2011?��̨��һģ������������ȷ���ǣ�������
��2011?��̨��һģ������������ȷ���ǣ�������