题目内容
4.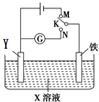 利用如图所示装置进行下列实验,下表中对应叙述正确的是( )
利用如图所示装置进行下列实验,下表中对应叙述正确的是( )| A | X为硫酸氢钠,Y为石墨 K与M连接时;K与N连接时 | 一段时间后溶液的pH均增大 |
| B | X为氯化钠,Y为石墨 K与M连接时; K与N连接时 | 石墨电极反应均为: 4OH--4e-═2H2O+O2↑ |
| C | X为硫酸氢钠,Y为锌 K与M连接时; K与N连接时 | 铁电极反应均为: 2H++2e-═H2↑ |
| D | X为氯化钠,Y为锌 K与M连接时; K与N连接时 | 铁电极的保护方法均为: 牺牲阳极的阴极保护法 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.X为硫酸氢钠,Y为石墨,K与M连接时,该装置是电解池,实质为电解水;K与N连接时,该装置是原电池,铁作负极,负极上铁失电子发生氧化反应,石墨作正极,正极上氢离子得电子发生还原反应;
B.X为氯化钠,Y为石墨,K与M连接时,该装置是电解池,石墨电极为阳极反应式为:2Cl--2e-═Cl2↑;K与N连接时,该装置是原电池,铁作负极,石墨作正极,铁发生吸氧腐蚀;
C.X为硫酸氢钠,Y为锌,K与M连接时,该装置是电解池,铁电极为阴极发生得电子的还原反应;K与N连接时,该装置是原电池,铁作正极发生得电子的还原反应;
D.X为氯化钠,Y为锌,K与M连接时,该装置是电解池;K与N连接时,该装置是原电池.
解答 解:A.X为硫酸氢钠,Y为石墨,K与M连接时,该装置是电解池,实质为电解水,使溶液浓度增大,所以酸性增强,pH值变小;K与N连接时,该装置是原电池,铁作负极,石墨作正极,正极上氢离子得电子发生还原反应,则溶液的氢离子浓度减小,所以pH值增大,故A错误;
B.X为氯化钠,Y为石墨,K与M连接时,该装置是电解池,石墨电极为阳极反应式为:2Cl--2e-═Cl2↑;K与N连接时,该装置是原电池,铁作负极,石墨作正极,铁发生吸氧腐蚀,正极反应为:2H2O+O2+4e-═4OH-,故B错误;
C.X为硫酸氢钠,Y为锌,K与M连接时,该装置是电解池,铁电极为阴极反应式为:2H++2e-═H2↑;K与N连接时,该装置是原电池,铁作正极,反应式为:2H++2e-═H2↑,故C正确;
D.X为氯化钠,Y为锌,K与M连接时,该装置是电解池,铁电极为阴极,铁电极的保护方法为:外接电流的阴极保护法;K与N连接时,该装置是原电池,铁作正极,铁电极的保护方法为:牺牲阳极的阴极保护法,故D错误.
故选C.
点评 本题考查原电池和电解池原理,易错选项是A,注意该反应中,实际上电解的是水,溶质的物质的量不变,而溶液的体积减小,所以溶质的物质的量浓度增大,为易错点.

 阅读快车系列答案
阅读快车系列答案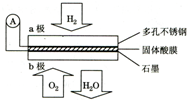
| A. | a极为负极,工作过程中a极附近酸性增强 | |
| B. | 电池总反应可表示为:2H2+O2=2H2O | |
| C. | H+由b极通过固体酸电解质传递到a极 | |
| D. | 每转移0.1mol电子,消耗标准状况下2.24L H2 |
| A. | 常温常压下,22.4L CO2中含有NA个CO2分子 | |
| B. | 常温下,1L 0.1mol/LNa2S溶液中,含有S2-数为0.1NA | |
| C. | 7.8 g过氧化钠与足量二氧化碳反应转移的电子数为0.1NA | |
| D. | 在反应KClO3+6HCl=KCl+3Cl2↑+3H2O中,每生成3 mol Cl2转移的电子数为6NA |
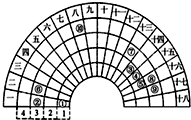 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法不正确的是( )
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法不正确的是( )| A. | 对应简单离子半径②>⑧>⑨ | |
| B. | 简单氢化物稳定性⑤>⑧ | |
| C. | 最高价氧化物对应的水化物酸性⑨>⑧>⑦ | |
| D. | ①分别与③、④、⑤均可形成既含极性键又含非极性键的化合物 |
| A. | CH3Cl | B. | C6H6 | C. | C6H12O6 | D. | CH3CHO |
 取两份10mL 1mol•L-1稀盐酸,向其中一份中加入过量的锌粒,得到气体的体积随时间变化如b所示,向另一份中加入过量的锌粒同时加入另一种物质,得到气体的体积如a所示,则另一种物质是( )
取两份10mL 1mol•L-1稀盐酸,向其中一份中加入过量的锌粒,得到气体的体积随时间变化如b所示,向另一份中加入过量的锌粒同时加入另一种物质,得到气体的体积如a所示,则另一种物质是( )| A. | 铝粉 | B. | 3 mol•L-1稀硫酸 | C. | 铁粉 | D. | 氢氧化钠固体 |
 有的油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示:
有的油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示: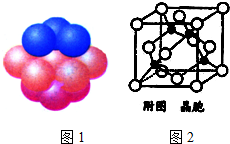 铁、铜及其化合物在日常生产、生活有着广泛的应用.请回答下列问题:
铁、铜及其化合物在日常生产、生活有着广泛的应用.请回答下列问题: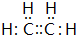 ;
;