题目内容
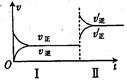
在密闭容器中,一定条件下进行反应:mA(g)+nB (g)  pC(g)+qD(g)。若增大压强或升高温度,重新达到平衡,随时间变化过程均如图所示,则对该反应的叙述中正确的是( )
pC(g)+qD(g)。若增大压强或升高温度,重新达到平衡,随时间变化过程均如图所示,则对该反应的叙述中正确的是( )
 pC(g)+qD(g)。若增大压强或升高温度,重新达到平衡,随时间变化过程均如图所示,则对该反应的叙述中正确的是( )
pC(g)+qD(g)。若增大压强或升高温度,重新达到平衡,随时间变化过程均如图所示,则对该反应的叙述中正确的是( )
| A.正反应是放热反应,m+n<p+q |
| B.逆反应是放热反应,m+n>p+q |
| C.正反应是放热反应,m+n>p+q |
| D.逆反应是放热反应,m+n<p+q |
A
试题分析:从图可以看出,改变条件逆反应速率大于正反应速率,说明平衡向逆反应方向移动,根据化学平衡移动原理分析,升温向吸热反应方向进行,故该反应为正反应是放热反应;增大压强平衡向气体体积减小的方向进行,则该反应的正反应为分子数增多的反应,所以m+n<p+q,故A正确,为本题的答案。
点评:本题考查了根据化学平衡的移动来判断化学反应的特点,属于逆向考查,该题有利于培养学生的分析能力,该题难度中等。

练习册系列答案
相关题目
 2 SO3(g)。已知反应过程某一时刻SO2、O2、SO3浓度(mol?L-1)分别为0.2、0.1、0.2,达到平衡时,浓度可能正确的是( )
2 SO3(g)。已知反应过程某一时刻SO2、O2、SO3浓度(mol?L-1)分别为0.2、0.1、0.2,达到平衡时,浓度可能正确的是( ) 2AB(g)达到平衡的标志是( )
2AB(g)达到平衡的标志是( )  2SCl2(l) ΔH=-50.16 kJ·mol-1
2SCl2(l) ΔH=-50.16 kJ·mol-1
 pC(g)+qD(g),
pC(g)+qD(g), 2SO3已经达到平衡状态的标志是
2SO3已经达到平衡状态的标志是 2Z2(g),若X2、Y2、Z2的起始浓度分别为0.1 mol/L、0.3 mol/L、0.2 mol/L,达到平衡时下列物质的浓度不可能为
2Z2(g),若X2、Y2、Z2的起始浓度分别为0.1 mol/L、0.3 mol/L、0.2 mol/L,达到平衡时下列物质的浓度不可能为 