题目内容
在一定温度下,4L密闭容器内M、N两种物质随时间变化的曲线如图所示:
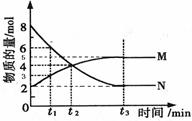
⑴由图中的数据分析,该反应的化学方程式为 。
⑵若t2 =2min,计算反应开始至t2时刻,M的平均化学反应速率为:_____。
(3)t3 min末N的正反应速率与 t3min后N的正反应速率相比 (填 “大”“小”或“相等”)。

⑴由图中的数据分析,该反应的化学方程式为 。
⑵若t2 =2min,计算反应开始至t2时刻,M的平均化学反应速率为:_____。
(3)t3 min末N的正反应速率与 t3min后N的正反应速率相比 (填 “大”“小”或“相等”)。
(1)2N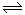 M (2)0.25mol/(L?min) (3)相等
M (2)0.25mol/(L?min) (3)相等
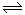 M (2)0.25mol/(L?min) (3)相等
M (2)0.25mol/(L?min) (3)相等试题分析:由图可以知道,达到平衡状态,N反应了6mol,生成了M为3mol,所以反应的化学方程式为2N
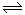 M;(2)若t2 =2min,M的平均化学反应速率为=(4-2)/4/2=0.25mol/(L?min);(3)t3 min时,该反应已经达到平衡,所以正反反应速率都相等。
M;(2)若t2 =2min,M的平均化学反应速率为=(4-2)/4/2=0.25mol/(L?min);(3)t3 min时,该反应已经达到平衡,所以正反反应速率都相等。点评:本题考查了化学方程式和化学平衡的基本计算,本题不难。

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
 pC(g)+qD(g)。若增大压强或升高温度,重新达到平衡,随时间变化过程均如图所示,则对该反应的叙述中正确的是( )
pC(g)+qD(g)。若增大压强或升高温度,重新达到平衡,随时间变化过程均如图所示,则对该反应的叙述中正确的是( )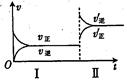
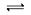 cZ(g)+dW(g)反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列叙述中不正确的是
cZ(g)+dW(g)反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列叙述中不正确的是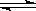 2NH3而言,无论怎样控制反应条件1mol N2与3mol H2反应都不会生成2mol NH3
2NH3而言,无论怎样控制反应条件1mol N2与3mol H2反应都不会生成2mol NH3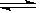 Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为( )
Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为( )
 2SO3(g),下列判断正确的是
2SO3(g),下列判断正确的是 C(g) +D(g) 反应过程中的能量变化如图所示,回答下列问题。
C(g) +D(g) 反应过程中的能量变化如图所示,回答下列问题。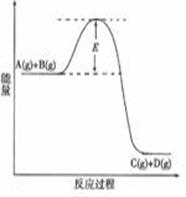
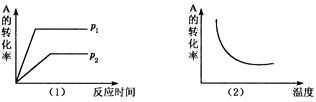
 x C(g),在不同温度及压强(p1, p2)条件下,反应物A的转化率如图所示,下列判断正确的是
x C(g),在不同温度及压强(p1, p2)条件下,反应物A的转化率如图所示,下列判断正确的是