题目内容
(1) 纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
2Cu(s)+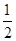 O2(g) ="==" Cu2O(s) ΔH=-169kJ·mol-1,
O2(g) ="==" Cu2O(s) ΔH=-169kJ·mol-1,
C(s)+ 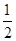 O2(g) ="==" CO(g) ΔH=-110.5kJ·mol-1,
O2(g) ="==" CO(g) ΔH=-110.5kJ·mol-1,
2Cu(s)+ O2(g)===2 CuO(s) ΔH=-314kJ·mol-1
则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
。
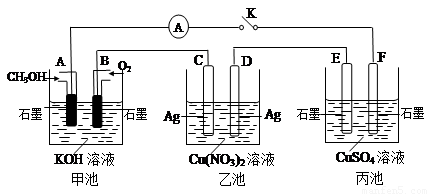
(2)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
请回答下列问题:
(1)甲池为 (填“原电池”、“电解池”或 “电镀池”),A电极的电极反应式为 。
(2)丙池中F电极为 (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为 。
(3)当池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为 mL(标准状况)。
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是 (填选项字母)。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(OH)2CO3 |
(1)C(s) + 2CuO (s)= Cu2O(s) + CO(g)  H =+34.5kJ·mol.-1(3分)
H =+34.5kJ·mol.-1(3分)
(2)①原电池 (1分) CH3OH + 8OH--6e- = CO32-+ 6H2O(2分)
②阴极(1分) 2CuSO4+ 2H2O  2H2SO4 + 2Cu + O2↑(2分)
2H2SO4 + 2Cu + O2↑(2分)
③560(2分)
④A(2分)
解析试题分析:(1)工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
C(s) + 2CuO (s)= Cu2O(s) + CO(g)  H =a,
H =a, H 的计算如下,C(s)+
H 的计算如下,C(s)+ 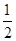 O2(g) ="==" CO(g) 减去2Cu(s)+ O2(g)===2 CuO(s) 再加上2Cu(s)+
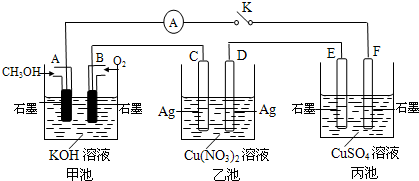
O2(g) ="==" CO(g) 减去2Cu(s)+ O2(g)===2 CuO(s) 再加上2Cu(s)+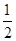 O2(g) ="==" Cu2O(s) 可以得到C(s) + 2CuO (s)= Cu2O(s) + CO(g) ,所以
O2(g) ="==" Cu2O(s) 可以得到C(s) + 2CuO (s)= Cu2O(s) + CO(g) ,所以 H =-110.5+314-169=+34.5kJ·mol.-1,所以工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
H =-110.5+314-169=+34.5kJ·mol.-1,所以工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
C(s) + 2CuO (s)= Cu2O(s) + CO(g)  H =+34.5kJ·mol.-1;
H =+34.5kJ·mol.-1;
(1)由图可以知道,甲池为原电池,A电极为负极,该电极反应式为CH3OH + 8OH--6e- = CO32-+ 6H2O;(2)丙池中F电极与电池的负极连接,所以F电极为阴极,丙电池为电解池,该电池的总的反应式为2CuSO4+ 2H2O  2H2SO4 + 2Cu + O2↑;(3)C极中,Ag溶解,所以当池中C极质量减轻10.8 g时,即通过的电子数为10.8/108=0.1mol,所以B电极理论上消耗O2的体积=0.1/4×22.4×1000=560mL;(4)一段时间后,断开电键K,乙池在电解的过程中引入了银离子,有一部分铜离子在电极上析出,所以加入Cu可以恢复到原来的浓度,故本题的答案选择A。
2H2SO4 + 2Cu + O2↑;(3)C极中,Ag溶解,所以当池中C极质量减轻10.8 g时,即通过的电子数为10.8/108=0.1mol,所以B电极理论上消耗O2的体积=0.1/4×22.4×1000=560mL;(4)一段时间后,断开电键K,乙池在电解的过程中引入了银离子,有一部分铜离子在电极上析出,所以加入Cu可以恢复到原来的浓度,故本题的答案选择A。
考点:热化学方程式的书写、原电池、电解池
点评:本题考查了热化学方程式的书写、原电池、电解池,这些考点是高考考查的重点和难点,本题有一定的综合性,难度适中。

(15分)纳米级Cu2 O 粉末,由于量子尺寸效应,其具有特殊的光学、电学及光电化学性质,在太阳电池、传感器、超导体、制氢和电致变色、环境中处理有机污染物等方面有着潜在的应用。
Ⅰ.纳米氧化亚铜的制备
(1)四种制取Cu2O的方法如下:
①火法还原。用炭粉在高温条件下还原CuO;
②最新实验研究用肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时放出N2。
已知:N2H4(l)+O2(g) N2(g)+2H2O(l)
△H=-a
kJ/mol
N2(g)+2H2O(l)
△H=-a
kJ/mol
Cu(OH)2(s) CuO(s)+H2O(l) △H=b kJ/mol
CuO(s)+H2O(l) △H=b kJ/mol
4CuO(s) 2Cu2O(s)+O2(g)
△H=c
kJ/mol
2Cu2O(s)+O2(g)
△H=c
kJ/mol
则该方法制备Cu2O的热化学方程式为 。
③工业中主要采用电解法:用铜和钛作电极,电解氯化钠和氢氧化钠的混合溶液,电解总方程式为:2Cu+H2O Cu2O+H2↑,则阳极反应式为:
。
Cu2O+H2↑,则阳极反应式为:
。
④还可采用Na2SO3还原CuSO4法:将Na2SO3 和CuSO4加入溶解槽中,制成一定浓度的溶液,通入蒸气加热,于100℃~104℃间反应即可制得。写出该反应的化学方程式: 。
Ⅱ.纳米氧化亚铜的应用
(2)用制得的Cu2O进行催化分解水的实验
①一定温度下,在2 L密闭容器中加入纳米级Cu2O并通入10. 0 mol水蒸气,发生反应:
2H2O(g)  2H2(g)+O2(g)
△H=+484 kJ·mol-1
2H2(g)+O2(g)
△H=+484 kJ·mol-1
T1温度下不同时段产生O2的量见下表:
|
时间/min |
20 |
40 |
60 |
80 |
|
n(O2)/mol |
1.0 |
1.6 |
2.0 |
2.0 |
前20 min的反应速率 v(H2O)= ;该该温度下,反应的平衡常数的表达式K= ;若T2温度下K=0.4,T1 T2(填>、<、=)
②右图表示在t1时刻达到平衡后,只改变一个条件又达到平衡的不同时段内,H2的浓度随时间变化的情况,则t1时平衡的移动方向为 ,t2时改变的条件可能为 ;若以K1、K2、K3分别表示t1时刻起改变条件的三个时间段内的平衡常数,t3时刻没有加入或减少体系中的任何物质,则K1、K2、K3的关系为 ;

③用以上四种方法制得的Cu2O在其它条件相同下分别对水催化分解,产生氢气的速率v随时间t变化如图所示。下列叙述正确的是 。

A.方法③、④制得的Cu2O催化效率相对较高
B.方法④制得的Cu2O作催化剂时,水的平衡转化率最高
C.催化效果与Cu2O颗粒的粗细、表面活性等有
D.Cu2O催化水分解时,需要适宜的温度
(1) 纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
2Cu(s)+![]() O2(g) === Cu2O(s) ΔH=-169kJ·mol-1,
O2(g) === Cu2O(s) ΔH=-169kJ·mol-1,
C(s)+ ![]() O2(g) === CO(g) ΔH=-110.5kJ·mol-1,
O2(g) === CO(g) ΔH=-110.5kJ·mol-1,
2Cu(s)+ O2(g)=== CuO(s) ΔH=-314kJ·mol-1
则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
。
(2)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
 |
请回答下列问题:
(1)甲池为 (填“原电池”、“电解池”或 “电镀池”),A电极的电极反应式为 。
(2)丙池中F电极为 (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为
。
(3)当池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为 mL(标准状况)。
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是 (填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
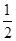 O2(g) ="==" Cu2O(s)
ΔH=-169kJ·mol-1,
O2(g) ="==" Cu2O(s)
ΔH=-169kJ·mol-1,