题目内容
某气态有机物标准状况下密度为1.34g/L,取1.50克该有机物在足量的氧气中燃烧.将所得气体通过装有浓H2SO4的洗气瓶后再通过碱石灰干燥管,洗气瓶和干燥管分别增重0.9克和2.2克,测得尾气中除氧气外无其它物质,则有机物是( )
| A、甲醛 | B、乙烯 | C、乙醛 | D、甲酸 |
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:某气态有机物标准状况下密度为1.34g/L,则该有机物的摩尔质量=1.34g/L×22.4L/mol=30g/mol,装有浓H2SO4的洗气瓶增重0.9g为生成水的质量,盛有碱石灰干燥管增重2.2克为二氧化碳的质量,根据n=
计算1.5g有机物、水、二氧化碳的物质的量,结合质量守恒判断有机物中是否含有氧元素,确定有机物最简式,结合相对分子质量确定有机物分子式.
| m |
| M |
解答:
解:某气态有机物标准状况下密度为1.34g/L,则该有机物的摩尔质量=1.34g/L×22.4L/mol=30g/mol,装有浓H2SO4的洗气瓶增重0.9g为生成水的质量,水的物质的量=
=0.05mol,
盛有碱石灰干燥管增重2.2克为二氧化碳的质量,其物质的量=
=0.05mol,
m(C)+m(H)=0.05mol×12g/mol+0.05mol×2×1g/mol=0.7g<1.5g,故有机物中含有O元素,1.5gg有机物中m(O)=1.5g-0.7g=0.8g,故n(O)=
=0.05mol,
故有机物中C、H、O原子数目之比=0.05mol:0.05mol×2:0.05mol=1:2:1,即有机物最简式为CH2O,有机物的相对分子质量为30,则最简式CH2O的相对分子质量为30,故最简式即为分子式,该物质为甲醛,
故选A.
| 0.9g |
| 18g/mol |
盛有碱石灰干燥管增重2.2克为二氧化碳的质量,其物质的量=
| 2.2g |
| 44g/mol |
m(C)+m(H)=0.05mol×12g/mol+0.05mol×2×1g/mol=0.7g<1.5g,故有机物中含有O元素,1.5gg有机物中m(O)=1.5g-0.7g=0.8g,故n(O)=
| 0.8g |
| 16g/mol |
故有机物中C、H、O原子数目之比=0.05mol:0.05mol×2:0.05mol=1:2:1,即有机物最简式为CH2O,有机物的相对分子质量为30,则最简式CH2O的相对分子质量为30,故最简式即为分子式,该物质为甲醛,
故选A.
点评:本题考查有机物分子式的确定,难度不大,关键是根据质量守恒进行有机物中氧元素的判断,注意掌握燃烧法利用原子守恒确定有机物分子式.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
下列表达方式错误的是( )
| A、HCl的电子式 H:Cl |
B、S2-的结构示意图是: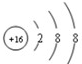 |
| C、O-18原子的符号:818O |
| D、CO2分子的结构式 O=C=O |
设NA为阿佛加德罗常数的数值,下列说法正确的是( )
| A、等物质的量的H2和N2所含分子数均为NA |
| B、标准状况下,11.2L的己烷含有分子数为0.5NA |
| C、常温常压下,46g NO2含有原子数为3NA |
| D、1mol SiO2晶体中含NA个SiO2分子 |
下列说法正确的是( )
| A、铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
| C、一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
| D、相同条件下,溶液中Cu2+、Fe3+、Zn2+的氧化性依次增强 |
在NH4HSO3溶液中逐滴加入Ba(OH)2溶液,下列离子方程式一定错误的是( )
| A、2HSO3-+Ba2++2OH-→BaSO3↓+SO32-+2H2O |
| B、NH4++HSO3-+Ba2++2OH-→BaSO3↓+NH3?H2O+H2O |
| C、NH4++3HSO3-+2Ba2++4OH-→2BaSO3↓+SO32-+NH3?H2O+3H2O |
| D、HSO3-+Ba2++OH-→BaSO3↓+H2O |
下列反应的离子方程式正确的是( )
| A、FeCl3溶液腐蚀铜板电路:Fe3++Cu=Fe2++Cu2+ |
| B、碳酸钙溶于醋酸溶液:CaCO3+2H+=Ca2++CO2↑+H2O |
| C、Ba(OH)2溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| D、铜与稀硝酸反应:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O |
下列离子方程式中正确的是( )
| A、向溶液Na2FeO4中加入稀H2SO4产生氧气:4FeO42-+2OH-=4Fe2++3O2↑+10H2O |
| B、向溶液NH4Al(SO4)2中滴入溶液Ba(OH)2恰好使(SO4)2-沉淀完全2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O |
| C、向溶液Mg(HCO3)2中加入过量的NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O |
| D、向溶液Fe(NO3)2中加入稀氢碘酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
 已知:2KMnO4+16HCl═2KCl+5Cl2↑+2MnCl2+8H2O,如图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.对实验现象的“解释或结论”正确的是( )
已知:2KMnO4+16HCl═2KCl+5Cl2↑+2MnCl2+8H2O,如图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.对实验现象的“解释或结论”正确的是( )